Nivel 4 - Patologías
CONCEPTO
ENCOPRESIS FUNCIONAL
- Descripción clínica
- Ettiología
- Evaluación
ENURESIS FUNCIONAL
- Descripción clínica
- Etiología
- Evaluación
Concepto
Los trastornos de la eliminación se caracterizan por la emisión de heces u orina en lugares inapropiados por un niño cuyo nivel de desarrollo le proporciona la capacidad de poseer control del intestino, vejiga y esfínteres. Este control de hábitos higiénicos está afectado por muchos factores: capacidad intelectual, madurez social e interacciones sociales entre el niño sus familiares y ámbito educativo. La secuencia normal del desarrollo de continencia fecal y urinaria implica tanto el control diurno como nocturno.
1 comentario
Este trastorno de la eliminación consiste en la evacuación de las heces en lugares inapropiados, tanto si es involuntario como intencionado. Este patrón conductual debe estar presente al menos durante tres meses y la edad evolutiva del niño no debe ser inferior a 4 años.
Es necesario excluir las causas orgánicas de la encopresis, por lo tanto, debe obtenerse una evaluación médica de las anomalías no funcionales antes de etiquetarla como funcional.
Criterios diagnósticos para la Encopresis (DSM-IV-TR)
A. Evacuación repetidas de heces en lugares inadecuados (p.ej., vestidos o suelos), sea voluntaria o intencionada.
B. Por lo menos un episodio al mes durante un mínimo de 3 meses.
C. La edad cronológica es por lo menos de 4 años ( o un nivel de desarrollo equivalente).
D. El comportamiento no se debe exclusivamente a los efectos fisiológicos directos de una sustancia (p.ej., laxantes) ni a una enfermedad médica, excepto a través de un mecanismo que implique estreñimiento.
Codificar del modo siguiente:
Con estreñimiento e incontinencia por rebosamiento
Sin estreñimiento ni incontinencia por rebosamiento
Descripción clínica
La encopresis funcional durante el día es más común que la encopresis nocturna. En la mitad de estos pacientes, el control intestinal no está todavía aprendido, por lo que el síntoma puede ser considerado como un reflejo de una fijación evolutiva temprana (encopresis primaria). En la otra mitad, los niños aprendieron inicialmente el control intestinal, han sido capaces de contener al menos durante un año, y luego se ha producido la regresión (encopresis secundaria). La encopresis secundaria empieza normalmente hacia los 8 años.
La encopresis sin estreñimiento ni rebosamiento puede implicar una variedad de fuentes, incluyendo una falta de conciencia o un pobre control. En caso de que el episodio ocurra después del baño, la estimulación física puede ser la causa. Si el episodio es deliberado, el niño es generalmente hostil o agresivo; debe entonces tenerse en cuenta el trastorno antisocial o un trastorno psiquiátrico mayor. El hecho de ensuciarse puede ser accidental (el niño trata de ocultarlo) o deliberado (desafiante). Ciertos niños encopréticos muestran síntomas neuroevolutivos, incluyendo falta de atención, hiperactividad, impulsividad, baja tolerancia a la frustración y descoordinación.
Los problemas de comportamiento tales como los trastornos de conducta son comunes en la población infantil psiquiátrica referida por problemas de encopresis, pero comparativamente pequeños en la muestra vista por pediatras. En población psiquiátrica, el 25% de los niños con encopresis funcional también presenta enuresis funcional.
Algunos niños ocultan tanto la orina como las heces, y pueden tener megavejiga y megacolon. Se observan con frecuencia dolores de estómago, largos períodos sentados en la taza del lavabo y estreñimiento crónico. En las niñas son frecuentes las infecciones del tracto urinario y la pielonefritis crónica. A menudo, los niños con encopresis funcional tienen vergüenza y turbación y presentan una baja autoestima. Pueden sufrir acusaciones de los padres y hermanos, pueden tener miedo a ser descubiertos por los compañeros, y se esconden física y emocionalmente.
Entre el 75 y el 90% de los casos implican el subtipo que el DSM-IV designa como “con estreñimiento e incontinencia por rebosamiento”. Estos casos retentivos incluyen una baja frecuencia de movimientos intestinales, impactación, rebosamiento de líquido alrededor del asiento habitual, y manchas de líquido en la ropa. Este tipo de encopresis puede ser debido a estreñimiento crónico, entrenamiento de los hábitos de higiene inadecuado (excesivamente coercitivo o perfeccionista), dolor (debido a fisura anal) o evitación fóbica de los lavabos. Estos episodios retentivos generalmente se extienden durante varios días y son seguidos de defecación dolorosa.
La encopresis funcional es menos común que la enuresis. La prevalencia es aproximadamente del 1,5% después de los cinco años, disminuye con la edad, y se produce raramente en los adolescentes. Las tasas ligeramente superiores están asociadas con las clases socioeconómicas más bajas. Existe un predominio masculino de 4:1. Se da una aparición familiar de la encopresis funcional, con el 15% de los padres que han sufrido encopresis en su niñez. Se han observado tasas más altas entre los individuos con retraso mental, especialmente en los casos moderados y graves.
Etiología
La encopresis con frecuencia es derivada de una compleja interacción ente factores fisiológicos y psicológicos. Entre los mecanismos fisiopatológicos se encuentran: una alteración del movimiento del colon y de los patrones de contracción, elasticidad y adelgazamiento de las paredes del colon (megacolon) y disminución de la sensación o percepción.
En la infancia, la encopresis puede ser resultado de una erupción cutánea debida al pañal, cuando se produce la retención fecal para evitar el dolor rectal. Estas causas médicas de manchas de heces excluyen el diagnóstico de encopresis funcional. La encopresis puede ser el resultado de un entrenamiento del control de esfínteres inadecuado o punitivo (doloroso, coercitivo, agresivo), de una alteración física asociada a una ayuda inadecuada durante el entrenamiento en el uso, del inodoro (si los pies no tocan el suelo), o de un manejo incorrecto de los miedos relacionados con el lavabo.
Los factores relacionados con el estrés parecen ser la causa de la mitad de los casos de encopresis secundaria. Existe una gran prevalencia de psicopatología individual y familiar en la encopresis funcional. Sin embargo, a diferencia de la enuresis, no existe la evidencia de un factor genético en la etiología de la encopresis, incluso en las formas familiares.
Evaluación
Es necesaria una evaluación médica inicial para descartar enfermedades médicas como el megacolon agangliónico o enfermedad de Hirschsprung y evaluar posibles anomalías estructurales (por ej., fisura anal), y puede suponer un enema de bario.
La evaluación psiquiátrica incluye una valoración de los trastornos psiquiátricos asociados, incluyendo el retraso mental, el trastorno de negativismo desafiante, el trastorno de conducta, los trastornos afectivos y las psicosis. No existen estudios longitudinales importantes, pero la psicopatología asociada a los trastornos médicos pueden ser la principal determinante del pronóstico. El trastorno disocial, el uso de la encopresis como una expresión directa de la ira y el desinterés de los padres hacia el problema, parecen predecir un curso complicado.
Tratamiento
El manejo fisiológico de los casos leves puede incluir la limpieza del intestino (laxantes, enemas), mantenimiento diario con aceite mineral, consejos (educación, reducción de los conflictos interpersonales y los efectos negativos, y recompensas) y seguimiento. En la práctica, aproximadamente del 50 al 75% de los casos mejora.
En los casos resistentes, está indicada una intervención psiquiátrica y psicológica individual y familiar. El centro del tratamiento cambia entonces de la atención a la encopresis a un tratamiento más general de los trastornos psicopatológicos asociados. La mayoría de los casos pueden ser tratados con tratamiento conductual, pero la psicoterapia de apoyo y las técnicas de relajación resultan muy útiles en el tratamiento de la ansiedad, baja autoestima y aislamiento social en los niños encopréticos. También son importantes las intervenciones familiares, para eliminar las tensiones de la familia y crear una atmósfera no punitiva. Estos esfuerzos también son necesarios en el ámbito escolar.
Se define como el vaciado repetido de orina en lugares inapropiados, tanto si el vaciado es involuntario como intencionado. Como un fenómeno evolutivo normal, en niños pequeños puede observarse incontinencia urinaria, y ocasionalmente en niños más mayores después de la conclusión del entrenamiento en el control de esfínteres. La enuresis funcional se diagnostica cuando la frecuencia de la incontinencia urinaria, sin explicación médica, sobrepasa las pautas evolutivas, es molesta o interfiere con las actividades cotidianas. El control de la vejiga de la orina se alcanza normalmente a los 3 o 4 años.
Criterios diagnósticos para la Enuresis (DSM-IV-TR)
A. Emisión repetida de orina en la cama o en los vestidos ( sea voluntaria o intencionada)
B. El comportamiento en cuestión es clínicamente significativo, manifestándose con una frecuencia de 2 episodios semanales durante por lo menos 3 meses consecutivos o por la presencia de malestar clínicamente significativo o deterioro social, académico (laboral) o de otras áreas importantes de la actividad del individuo.
C. La edad cronológica es de por lo menos de 5 años ( o el nivel de desarrollo equivalente)
D. El comportamiento no se debe exclusivamente al efecto fisiológico directo de una sustancia ( p.ej., un diurético), ni a una enfermedad médica (p.ej., diabetes, espina bífida, trastorno convulsivo).
Especificar tipo:
Sólo nocturna
Sólo diurna
Nocturna y diurna
El diagnóstico del DSM-IV requiere una edad mínima de 5 años. Antes de designar a estas presentaciones como funcionales, es necesaria una valoración médica de las causa físicas de la enuresis. A diferencia de la encopresis funcional, una vez se han descartado etiologías médicas y anatómicas, la enuresis funcional puede ser debida a trastornos neuroevolutivos, o del sueño, así como a trastornos psicológicos.
Descripción clínica
La enuresis nocturna aparece normalmente de 30 minutos a 3 horas después de iniciarse el sueño, estando el niño dormido a lo largo del episodio, o habiéndose despertado por la humedad. Sin embargo, para algunos niños, la enuresis puede ocurrir en cualquier momento de la noche. Los niños con enuresis diurna normalmente también sufren enuresis nocturna. En el 80% de los casos, todavía no se ha alcanzado el control de la vejiga, y la enuresis es primaria (debido a un trastorno neuromédico o a un retraso en el aprendizaje del control de la vejiga). En el 20%, la incontinencia urinaria es secundaria, y reaparece después de haberse alcanzado un funcionamiento competente (aparentemente, debido a un proceso interactivo).
Los síntomas de la enuresis funcional, a cualquier edad pueden conducir a la turbación, ira y castigo de los educadores, a la burla de los compañeros, a la evitación de campamentos y visitas en las que se pernocta, al retraimiento social y a las explosiones de ira. Estas complicaciones, si no se manejan correctamente, pueden tener un mayor impacto en el resultado a largo plazo que la enuresis por sí misma.
Se puede observar enuresis nocturna en el 25% de los chicos, pero aparece repetidamente después de los 5 años en el 7% al 10% de los chicos y en el 3% de las chicas. El predominio masculino se mantiene pero disminuye con la edad. A los 10 años, el 3% de los chicos y el 2% de las chicas son diagnosticables. La prevalencia general en la edad adulta es del 1%. No se ha establecido una correlación con el estatus socioeconómico.
Etiología
Se cree que la enuresis puede ser producida por múltiples etiologías. Las enuresis no funcionales pueden producirse por factores urológicos (infección de la vía urinaria, especialmente en el caso de la enuresis secundaria en chicas, u obstrucción), factores anatómicos (enfermedad espinal, vejiga o musculatura secundaria débil), factores fisiológicos (umbral anormalmente bajo de presión de la vejiga, lo que conduce a un vaciado anticipado), factores metabólicos (diabetes), o mecanismos neurológicos (trastornos convulsivos).
En las familias pueden observarse algunas formas de enuresis funcional especialmente en los varones. Aproximadamente el 70% de estos niños tiene un familiar en primer grado con enuresis funcional. La probabilidad de que un niño padezca enuresis es del 77% si ambos progenitores presentan una historia de enuresis, y del 44% si sólo la presenta uno de ellos.
Para muchos niños y adultos con enuresis nocturna la causa puede hallarse en factores hormonales o de ritmos biológicos. Algunos niños con enuresis nocturna no tienen una liberación normal de vasopresina durante la noche y pueden no tener la habitual disminución nocturna de producción de orina. Este hecho es el fundamento del tratamiento farmacológico con desmopresina, un análogo de la vasopresina.
Un trastorno del sueño puede ser un factor etiológico de la enuresis funcional para una minoría de casos. Todavía se debaten los hallazgos del EEG; parece ser que al menos algunos episodios de enuresis aparecen en cualquier fase del EEG, pero es posible que exista una concentración de episodios durante el sueño delta (fase 3 y 4; no REM) o durante el arousal post-delta (la transición de delta hacia el sueño REM).
En algunos casos se ha sugerido que se trata de un trastorno madurativo debido a los hallazgos del pequeño volumen de las evacuaciones, la corta estatura, la edad ósea media baja comparada con la edad cronológica y, en la adolescencia, un retraso de la maduración sexual.
Aproximadamente la mitad de los niños con enuresis funcional presentan síntomas emocionales o conductuales, pero está poco claro si esto representa una causa, un efecto o un hallazgo asociado (por ejemplo, limitación del entorno poco clara por parte de los padres). La enuresis funcional puede estar también relacionada con el estrés, los traumas, o las crisis psicosociales como el nacimiento de hermanos, comienzo de la escuela, traslados, hospitalización, pérdida, ausencia paterna o crisis de desarrollo. En estos casos de enuresis secundaria inducida por el estrés, existe igual prevalencia en chicos que en chicas.
La enuresis intencional puede implicar psicopatología, pero puede ser difícil de identificar en casos individuales o en acontecimientos aislados (especialmente si los episodios voluntarios son utilizados para camuflar o encubrir acontecimientos no intencionales).
La enuresis funcional tiene una tasa de remisión espontánea del 15% anual. Aproximadamente el 1% de los chicos (menos en las chicas) presentan todavía este estado a los 18 años, generalmente con poca psicopatología asociada. Sin embargo, la enuresis que se inicia en la adolescencia puede significar una mayor psicopatología y un resultado menos favorable.
Evaluación
Es necesaria una valoración médica para descartar las diversas formas no funcionales u orgánicas de la enuresis. Las manifestaciones orgánicas están relacionadas con patología genitourinaria: estructural, neurológica e infecciosa, como uropatía obstructiva, espina bífida oculta y cistitis. Otros trastornos orgánicos que pueden cursar con poliuria y enuresis son: diabetes mellitus, diabetes insípida, trastornos de conciencia y del sueño, intoxicación, sonambulismo y como efecto secundario de antipsicóticos, por ejemplo tioridacina.
Puede ser útil una evaluación del sueño, si bien no se requiere un EEG de forma rutinaria. Puede ser útil la medida de determinados índices madurativos para identificar la evolución del desarrollo. La evaluación psiquiátrica del niño y de la familia incluye una valoración de la psicopatología asociada, de los estresores psicosociales recientes, y una evaluación de la preocupación de la familia y del manejo de los síntomas.
Tratamiento
Los tratamientos más exitosos incluyen las intervenciones conductuales y farmacológicas. El primer paso ante cualquier tratamiento es revisar la utilización del inodoro adecuadamente, ya que si no se ha realizado el entrenamiento, los padres y el niño deben ser dirigidos en el proceso.
Dentro del tratamiento psicológico, el condicionamiento clásico se ha evidenciado como efectivo y es igualmente rápido y eficaz en niños con trastorno psiquiátrico concomitante que sin él. Este método conductual incluyen: el entrenamiento de los esfínteres, despertar al niño en la mitad del sueño para que vaya al lavabo, y recompensas por no mojar la cama. Generalmente se utiliza un aparato que hace sonar un timbre conectado a la ropa, sensible a la humedad para despertar al niño cuando se orina (pipi-stop). Presenta una tasa de éxito (sobre el 80%), aunque también presenta una alta tasa de recaída (de hasta el 20%), que remite tras volver a iniciar el proceso. En único problema es el incumplimiento, y la falta de colaboración de los padres, necesaria cuando el niño es más pequeño.
El manejo de la vergüenza y la evitación que suele acompañar a este trastorno es una parte crítica del tratamiento cognitivo de estos niños. En general, es útil dejar de lado la explicación consciente o in consciente que puede engendrar la vergüenza o la culpa y atacar directamente el síntoma.
A nivel psicofarmacológico, los antidepresivos a dosis bajas pueden ayudar si un caso es resistente a las intervenciones conductuales, si se produce enuresis diurna y nocturna, o si aparece junto con un trastorno afectivo o un trastorno de ansiedad. Aunque algunos informes sugieren que la tasa de éxito es sólo de un 15% después de suprimir los antidepresivos, ésta es mucho mayor si la dosis se retira gradualmente. Se desconoce el mecanismo del tratamiento antidepresivo de la enuresis, pero no es debido a propiedades anticolinérgicas (ya que los agentes anticolinérgicos no son eficaces) y pueden estar relacionados con la propiedad antidepresiva (ya que los inhibidores de la monoaminooxidasa resultan eficaces).
La desmopresina, un análogo de la hormona antidiurética vasopresina, ha resultado eficaz para el tratamiento de la enuresis en varios estudios realizados a doble ciego. Su eficacia no es tan alta como la del aparato de alarma (pipi-stop), pero la combinación de ambos tratamientos parece la solución más efectiva. La desmopresina puede ser más efectiva en niños mayores, especialmente aquellos en los que se ha demostrado un descenso nocturno de la vasopresina.
Es esta sección vamos a tratar diferentes discapacidades de tipo psíquico que son provocadas o tienen su origen en una alteración de tipo genético y se expondrás los tratamientos que se utilizan en la actualidad para el tratamiento de las enfermedades o trastornos que provocan discapacidad psíquica de origen genético.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
El presente informe ha sido realizado por la Federación Española del Síndrome X Frágil, inscrita en el Registro Nacional de Asociaciones con el número F 2124.
Este trabajo es producto de la compilación de la documentación disponible por la Federación. Los términos, descripciones, conceptos, consejos, proceden de dicha documentación.
Introducción
Un síndrome, en medicina, es un conjunto de signos y síntomas que existen al mismo tiempo y que definen clínicamente un estado de enfermedad. En el caso del síndrome X-Frágil, la causa de estos síntomas viene dada por una anomalía en un cromosoma sexual X.
Un tipo especial de retraso mental hereditario ligado al sexo ya fue descrito en los años cuarenta por Martin y Bell (1943) y posteriormente por Renpenning et al.(1962), a partir del estudio clínico de familias con diversos casos de retraso mental en varones.
El correlativo citogenético de esta enfermedad, descubierto por Lubs en 1969, fue definido como una fragilidad en el brazo largo del cromosoma X. El actual nombre de síndrome X-Frágil lo introdujo diez años después G.R. Sutherland (1979).
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
Cada persona posee 23 pares de cromosomas. Una de estas parejas determina el sexo con el que se nace, adoptando el nombre de “cromosomas sexuales”. Por su forma se identifican los cromosomas sexuales femeninos (determinan que la persona sea de sexo femenino) como XX, y la pareja de cromosomas masculinos como XY (determinan que la persona sea de sexo masculino).
A continuación se muestra la figura de un cariotipo de una mujer, identificado por los dos cromosomas X en la esquina inferior derecha.

Por tanto, las mujeres pueden tener esta anomalía en cualquiera de los dos cromosomas sexuales X, mientras que los hombres pueden padecerlo sólo en el único cromosoma sexual X que poseen.
La anomalía es debida a una mutación genética del ADN que afecta tanto a las células sexuales (óvulos y espermatozoides) como a los otros tipos de células de nuestro organismo.
Se sabe en la actualidad que esta mutación es producida inicialmente por el exceso de repetición de una tripleta de bases nitrogenadas: concretamente la CGG (Citosina, Guanina, Guanina). Ello hace que se produzca en exceso lo que en química se llama grupos de metilo (se produce una hipermetilación en la zona llamada “isla CpG”), dañando principalmente al gen situado en el locus Xq.27.3 (final del brazo largo del cromosoma X), que está junto al locus afectado de la hipermetilazión, influyendo definitivamente también a la proteína (cromatina) que envuelve al cromosoma X que en este locus se ve disminuida haciendo más frágil al cromosoma.
Este gen se ve anulado y no puede ejercer su función, fabricar la proteína llamada FMR-1-P, que ha sido identificada en diferentes tejidos, sobre todo las neuronas, y de la cual se sabe que juega un papel importante en el normal desarrollo del cerebro.
En la imagen siguiente se indica el lugar donde se localiza el gen FMR-1 (Fragile X Mental Retardation) (gen del retraso mental por X frágil).

Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
La mutación del cromosoma sexual X no se produce de golpe, sino que suele seguir un proceso que puede abarcar varias generaciones de una misma familia.
La mejor manera de explicar el proceso es partir del número de repeticiones de la tripleta CGG. Atendiendo a este criterio, podemos encontrar tres posibles estados del cromosoma X:
Normalidad: un cromosoma X no afectado suele presentar entre 5 y 50 repeticiones de la tripleta CGG en el locus en cuestión.
Premutación o predisposición: las repeticiones suelen estar entre 50 y 200, permitiendo al gen ser aún funcional y fabricar la proteína que le corresponde. En este caso se habla de mujeres portadoras y hombres transmisores normales.
Mutación completa: en este caso las repeticiones son más de 200 y pueden llegar a varios miles. La mutación o las repeticiones de la tripleta CGG se modifican cuando se transmiten de padres a hijos y tienden a aumentar en mayor medida cuando la premutación pasa a través de la mujer. Este cambio explica la mutación del cromosoma X frágil que se puede encontrar en una persona intelectualmente normal.
Actualmente se sabe que el estado de premutación es inestable durante la formación de la célula germinal femenina (óvulo), expandiéndose a mutación completa en la siguiente generación donde pueden nacer hijos afectados.
En el caso de los varones, la premutación es estable en la formación de espermatozoides (espermatogénesis) y permanece como tal en sus hijas, que siempre son normales; pero éstas podrían tener hijos afectados en los que la premutación se expandiría a mutación completa (es el fenómeno llamado “anticipación genética” o “paradoja de Sherman”).
Como influye el sexo de las personas
Existen diferencias importantes derivadas del sexo en dos aspectos principales:
- Afectación: como los cromosomas sexuales femeninos son XX, las mujeres tienen una defensa adicional importante que provoca que se vean menos afectadas: si uno de los cromosomas X tiene la mutación, siempre tienen el otro cromosoma X que puede suplir y tapar la anomalía de su par. En cambio, los hombres tienen un solo cromosoma X (el otro es el Y), por lo que la mutación en el cromosoma sexual X no puede ser suplida por ningún otro, y la afectación será casi segura.
- Herencia: las consecuencias de estar afectados respecto a los descendientes son diferentes según sea el padre o la madre quien sea el portador.
El padre portador puede transmitir el cromosoma X afectado a sus hijas pero nunca a sus hijos, pues a éstos les transfiere el cromosoma Y.
La madre portadora, tiene la probabilidad del 50% de transmitir el gen frágil X a cada uno de sus hijos o hijas.
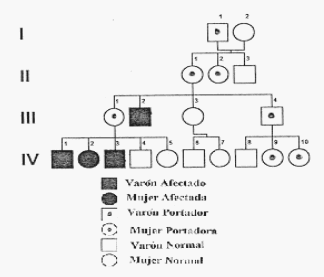
Ejemplo Genealógico del Síndrome
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
El test de laboratorio más frecuente usado ha sido el análisis citogenético, llamado también análisis cromosómico, que normalmente se efectúa con células de muestras de sangre (linfocitos). En ella se puede obtener una imagen del cromosoma X más o menos nítida y observar si existe un punto frágil o una rotura en el locus estudiado (Xq27.3). Esta característica no se puede observar en todas las células, sino que sólo se ve entre un 4 y un 50% de las estudiadas. En todo caso, mediante este análisis no se pueden observar los genes y, por lo tanto, es muy difícil apreciar los estados de premutación, por lo que no se detectará en la mayoría de las mujeres portadoras y los varones transmisores normales.
Posteriormente surgió la técnica de los estudios de enlaces de ADN, pero requerían análisis sanguíneos de múltiples miembros de la familia.
A partir de 1.992, una nueva técnica mucho más eficaz que la anterior en la detección de la anomalía es la del uso del método directo de análisis de ADN, mediante el cual se puede visualizar la extensión de las repeticiones de las tripletas CGG con exactitud y así detectar mutaciones y premutaciones. Esta técnica permite detectar tanto en varones como en mujeres, a individuos sanos, afectos y portadores, tanto pre como postnatalmente, lo que permite un asesoramiento genético de gran eficacia.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
Las cifras de incidencia en la población convierten al Síndrome X Frágil en la primera causa hereditaria de retraso mental y la segunda cromosopatía en frecuencia (después del Síndrome de Down). Aunque en nuestro país no existe una estadística al respecto, se estima que su frecuencia es de 1 individuo afectado por cada 4.000 nacimientos, una portadora por cada 800 y un portador por cada 5.000. Por ello, globalmente en España puede haber 8.000 varones portadores normales, 10.000 afectados por el retraso mental causado por el Síndrome X Frágil y 50.000 mujeres portadoras del cromosoma X frágil. Aproximadamente entre el 80-90% del total falta por diagnosticar.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
Hasta ahora se han descrito las causas genéticas del síndrome X Frágil. Los efectos, que más adelante se expondrán, son variados siendo el más importante el retraso mental, que oscila de leve a severo.
Aunque cada persona es diferente, hay una serie de síntomas comunes que se han observado en personas que padecen este síndrome.
Rasgos físicos
Los varones afectados por el síndrome X Frágil tienen como rasgos físicos más característicos macroorquidismo o testículos grandes (80% de los varones adultos), orejas grandes y prominentes (80% de los casos), cara larga y estrecha, mandíbula inferior prominente y problemas de infecciones en el oído medio.
Aproximadamente un 60% de los varones presentan hipersensibilidad en las articulaciones. Esto se detecta doblando los dedos hacia atrás en dirección a los nudillos. También los pies planos aparecen en un 50% de los niños y adultos.
Otros rasgos son el estrabismo que se detecta en un 25-50% de los casos y prolapso en la válvula mitral que se presenta en el 80% de los adultos (en el ANEXO I de este informe se acompaña un trabajo realizado por la doctora Esther Rodríguez Adrada, donde se hace una descripción más detallada de este problema).
En cuanto a mujeres con síndrome X frágil los síntomas son semejantes a la de los varones. Las que no se encuentren afectadas muestran algún rasgo físico propio del síndrome.
Comportamiento
La hiperactividad y falta de atención son problemas de conducta que se presentan tanto en varones como mujeres afectadas por el síndrome. Lenguaje desordenado y repetitivo, pobre mantenimiento de los temas, pensamientos expresados de forma incomprensible son características comunes.
Se han descrito en varones, rasgos que se han calificado como autistas. Mantenimiento escaso de la mirada, timidez, aleteos con las manos, repetición de la misma frase constantemente, aversión a ser tocado o abrazado, rabietas injustificadas, morderse las manos, se presentan en alrededor del 16% de los varones con X frágil.
Normalmente, los niños X frágil son cariñosos aunque los rasgos autistas interfieran con la relación normal.
Las mujeres afectadas por el síndrome, suelen presentar leve retraso mental, problemas de atención pero normalmente sin hiperactividad. Lo más frecuente es la timidez que puede ser profunda en la adolescencia, pudiendo llevar a depresión.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
En la actualidad, no hay cura para el síndrome X frágil, aunque se están desarrollando experimentos basados tanto en terapia genética como en ingeniería genética consistentes en reproducir la carencia de la proteína causante de la enfermedad.
No obstante, su tratamiento puede ayudar a los niños a alcanzar su máximo potencial. Esta ayuda puede ser tanto a nivel médico para los problemas que anteriormente se han descrito, como educacionales y de ocupación.
Tratamientos farmacológicos
Existen numerosos fármacos que pueden ayudar al control de la sintomatología, aunque la base de su utilización no es matemática y hay que "probar" hasta encontrar la que más se adecue individualmente según la sintomatología que presente, así como la dosis óptima, e ir revisándola muy de cerca para adaptarla a los cambios que vayan surgiendo en la patología del niño y el ambiente en el que se desarrolla.
En ocasiones se utiliza más de una medicación, para tratar una serie de problemas o por los efectos sinérgicos de las mismas, los efectos secundarios deben ser monitorizados cuidadosamente para que no lleguen a superar a los beneficios, también es útil recordar que la medicación no es el único tratamiento de este síndrome, como veremos más adelante, pero en la mayoría de los casos, como en las modificaciones de conducta estas intervenciones psicológicas son más efectivas con medicación.
Tratamiento psicopedagógico y conductual
Se debe tener en cuenta que como en cualquier síndrome, en el Frágil X, no todos los rasgos asociados están siempre presentes en todos los que lo padecen, siendo por tanto necesario en primer lugar saber las necesidades y habilidades del niño en concreto. Con frecuencia estos pacientes tienen habilidades para la imitación, la memoria visual, el humor y son prácticos a la hora de resolver un problema y aprender. La debilidad más común es la incapacidad para organizar la información y actuar sobre la misma de una forma efectiva. Teniendo en cuenta esto, los niños frágil X, necesitan apoyo en unas áreas determinadas:
- Atención, hiperactividad e impulsividad.
- Aprendizaje.
- Habla y lenguaje.
- Incapacidad para procesar la información sensorial de manera efectiva y habilidades motoras escasamente desarrolladas.
- Problemas de comportamiento.
Se observan grandes dificultades en el proceso auditivo, procesos secuenciales, razonamiento abstracto y habilidades aritméticas. La generalización es difícil y muchas veces una tarea o un concepto tiene que ser enseñado de varias formas para que el niño verdaderamente lo aprenda y sea capaz de manejar la información con sentido.
Las recomendaciones más frecuentes son:
- Control médico para los problemas de atención y comportamiento.
- Técnicas de autogobierno del comportamiento que incluyen:
- Fijar la meta, autocontrol, autorreforzamiento y ajuste de metas.
- Ayuda a los padres a entender los retrasos en el desarrollo de sus hijos, que en ocasiones es la tarea más difícil, así como sus comportamientos anormales. Debemos enseñarlos para que utilicen estrategias para estructurar el entorno, fomentar y facilitar la producción de habla y lenguaje, prevenir la sobreestimulación, utilizar técnicas terapéuticas calmantes y técnicas de reforzamiento positivo de la conducta.
- Terapia tanto para el habla como para el lenguaje, así como terapia para desarrollar el vocabulario y el lenguaje social. Estos niños presentan lenguaje acelerado, con ritmo desordenado, dispraxia verbal, articulación pobre, perseverancia, habla tangencial, falta de sencillez y naturalidad.
- Técnicas de integración sensorial.
- Servicios de educación especial, incluyendo un entorno educativo de apoyo que permita la modificación del formato instructivo y del plan de estudios.
- Utilizar materiales visuales que el niño pueda usar para aprender nuevas habilidades y rutinas.
- Utilizar materiales y temas que tengan gran interés para el niño, y así aprenderá con los objetos que realmente le gusten, se deben usar además objetos o fotografías de la vida real y dejar tiempo para que el niño responda y formule preguntas.
- Hacer que el niño participe en actividades de pequeños grupos. La imitación es buena para que adquiera un lenguaje social y un comportamiento adecuado. Además esta es una cualidad casi constante en ellos.
- Las dificultades en el proceso auditivo debe considerarse y la información que se le trasmite al niño tiene que ser en frases cortas y simples.
- Debemos ir modificando el material pedagógico para que siempre esté a la altura del desarrollo del niño y que le dé el apoyo suficiente para que consiga el éxito por el que está trabajando. La demostración y la repetición de las áreas son muy útiles para enseñar nuevas habilidades y rutinas.
Lo más importante de todo es que todas aquellas personas que estén trabajando con el niño deben perseguir el mismo propósito, por lo que es fundamental una coordinación en el trabajo entre los padres, profesores, psiquiatras y psicólogos, conociendo al niño y aprovechando todas aquellas cualidades que le pueden ser útiles e intentando modificar las que le interfieran con un buen funcionamiento psico-social.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
Debido a que los síntomas del X Frágil pueden ser bastante sutiles, especialmente en niños jóvenes y al hecho que el X Frágil tiene una incidencia notable en la población, muchos especialistas médicos recomiendan que la prueba sea tenida en cuenta para cualquier persona con atraso en el desarrollo o retraso mental de origen desconocido.
El diagnóstico prenatal debe ser realizado a toda aquella persona en cuya familia se haya detectado algún miembro con problemas de retraso mental.
El diagnóstico del síndrome de X frágil no se hace por la presencia de rasgos físicos. Cualquier demostración de retraso mental, una historia familiar de retraso mental o dificultades de aprendizaje de etilogía desconocida en combinación con alguna de las características anteriormente expuestas, pueden hacer sospechar que nos encontramos con un niño X frágil.
Se quiere resaltar de nuevo el que la única técnica fiable para detectar este trastorno genético es la que analiza directamente el ADN. Los estudios citogenéticos ofrecen un porcentaje elevado de falsos negativos.
Para ayudar y orientar a las familias en las que en su seno se haya diagnosticado algún caso de Síndrome X Frágil, se han creado Asociaciones sobre el Síndrome X Frágil en diferentes Comunidades del Estado, que se han integrado en una Federación Nacional.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
PUBLICACIONES DE INTERÉS EN ESPAÑOL
de Diego Otero Y., Pintado E., Hmadcha A., y Carrasco M.: Síndrome X Frágil y discapacidad mental hereditaria. Ministerio de Sanidad y Consumo (1999).
Ramos F.: El Síndrome X Frágil, material educativo de la Fundación Nacional del X Frágil de Estados Unidos. Traducción al español de material publicado bajo los auspicios de The National Fragile X Foundation en USA. Instituto de Migraciones y Servicios Sociales. Número 53 de la Colección Rehabilitación (1998).
BIBLIOGRAFÍA CIENTÍFICA
Biancalana V.; Taine1 L.; Bouix, J.C. y col.: Expansion and methylation status at FRAXE can be detected on EcoRI blots used br FRAXA diagnosis: analysis of four FRAXE families With mild mental retardation in males. Am J Hum Genet. Od, 59(4): p847-541 1996.
Carbonell, P.;López, I.; Gabarrón, J y col.: FRAXE mutation analysis in three Spanish families. Am. J. Med Genet. 64:434-440,1996.
Castellvi-Bel1 S.; Milá, M.; Soler, A. y col : Prenatal diagnosis of fragile X syndrome: (CGG)n expansion and methylation of chorionio vilus samples. Prenat-Diagn. Sep; 15(9): 801-7,1995.
Hagerman, R J.; Cronister, S: The fragile X syndrome 2ª edición. University press. 1996.
Hallmayer, J.; Pintado, E.; Lotspeich, L.; y col.: Molecular analysis and test of linkage between the FMR-1 gene and infantile autism in multiplex families Am. J. Hum. Genet. Nov; 55(5): 951-9, 1994.
Hmadcha, A; De Diego, Y.; Pintado, E: Assesment of Fmr-1 expression by RT-PCR of KH domains. J Lab Clin Med. 131(2): 170-173,1998.
Mila, M.; Castellvi-Bel, S; Sánchez, A; Lazaro. C; Villa M.; Estivill, X.: Mosaicism for the fragile X syndrome full mutation and deletions within the CGG repeat of the FMRI gene. J Med Genet Apr. 33(4): p338-40, 1996.
Pascual Pascual, S.I.; Garcia Marcos, J.A.; Martin Lucas, M.A.: Estudio del síndrome X-frágil en la población de la compañía telefónica de España. Rev. Neurol. May-Jun; 23(121): 644-7, 1995.
Pintado, E; de Diego, Y.; Hmadcha, A.; Carrasco1 M.; Sierra, J.; Lucas L.: Instability of the CGG repeat at the FRAXA locus and variable phenotypic expression in a large fragile x pedigree. J. Med. Genet 32: 907-908, 1995.
Turner, G.; Webb, T.; Wake, S.; Robinson, H.: Prevalence of fragile X syndrome. Am J Med Genet. Jul 12,64(1): p 196-7, 1996.
Willemsen, R.; Mohkamsing, S.; De Vries, B.; y col.: Rapid antibody test for fragile X syndrome Lancet 345: 1147-1148,1995.
Bibliografía Divulgativa:
- Aguirre, A. y Femández-Rua, J. M.: "La neurociencia proyecta rayos de luz sobre numerosos desórdenes del cerebro". ABC de la Ciencia 27 de marzo de 1998
- Borrero, J: ABC de la Sanidad. ABC de Sevilla. 10 de Abril de 1997.
- Carrasco, M., Pintado, E. Lucas, L., M De Diego, Y. Hmachda, A.: Intentemos prevenir lo que hoy no podemos curar: La deficiencia mental ligada a la fragilidad del cromosoma X. Revista Clave. Real patronato de prevención y atención a personas con minusvalías. Madrid 1996
De Diego Y.: Síndrome X Frágil Edición de bolsillo. Libro publicado por I Jornada Andaluza sobre el Síndrome X Frágil. Sevilla, 13 Julio 1998.
López. M.: El Síndrome del X Frágil: La causa más común de subnormalidad en el Hombre. Mundo Científico, Nº. 141, vol 13: 1066-1068.
Pintado E., de Diego Y., Hmadcha A., y Lucas M.: Diagnóstico Molecular del Síndrome X Frágil. Capítulo 10 del libro Diagnóstico Molecular en Genética Médica. Sociedad Española do Bioquímica Clínica y Patología Molecular. Dirigido por Lucas. M (1998).
Ramos, F. J: EI Síndrome X Frágil Material educativo de la Fundación Nacional del X Frágil de Estados Unidos". Editado por IMSERSO 1998 Número 53. Colección Rehabilitación.
Ruiz. M J. y Gómez-Ferrer, C.: Revisión de los tratamientos en el Síndrome Frágil X. Revista Electrónica de Psiquiatría Vol 1, Nº. 4. Diciembre 1997.
(La lista de bibliografía relacionada, ha sido obtenida del libro: Síndrome X Frágil. Edición de bolsillo. Libro publicado para la I Jornada Andaluza del Síndrome X Frágil).
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
1. Configuración y funcionamiento cardiaco
EI corazón es el órgano central del aparato circulatorio, formado por músculo y semejante a una bomba impulsora. En realidad está constituido por dos bombas separadas por un tabique, dividiendo así al corazón en dos partes laterales.
- Corazón derecho, por el que circula la sangre sin oxígeno (venosa)
- Corazón izquierdo, en relación con sangre oxigenada (arterial)
A su vez, cada una de estas dos mitades laterales se subdividen en otras dos, una superior llamada aurícula y otra inferior o ventrículo.
Ahora bien, así como los dos corazones están enteramente separados uno del otro, cada una de las aurículas comunica ampliamente con el ventrículo correspondiente del mismo lado por medio de un ancho orificio denominado auriculo-ventricular provisto de una aparato mecánico llamado válvulas, que en el corazón izquierdo se denomina mitral y en el derecho tricúspide, regulando el curso de la sangre. Estas descienden en el momento de la relajación cardiaca, dejando, que la sangre pase la aurícula al ventrículo, y se elevan durante la contracción cardiaca para evitar que esta misma sangre vuelva a ascender hasta la aurícula. (T1)
2. Circulación
El ventrículo izquierdo bombea sangre arterial penetrando en la arteria Aorta, la cual es la que se encarga de distribuirla a todos los órganos del cuerpo, cediéndoles oxigeno y tomando de ellos sustancias de desecho transformándose así en sangre venosa. Ésta a través de las venas llega a la aurícula derecha y pasa al ventrículo derecho por la válvula; el ventrículo derecho lo impulsa a la arteria pulmonar, llegando la sangre hasta los pulmones donde se despoja de su ácido carbónico y se carga con oxigeno, volviendo a tomar camino hacia el corazón, introduciéndose en la aurícula izquierda y por medio de su válvula al ventrículo izquierdo comenzando de nuevo el ciclo. (T2).
3. Prolapso de la válvula mitral
Síndrome clínico que afecta frecuentemente a personas entre los 15 y 30 años. En la mayoría de los pacientes se desconoce la causa, asociado también a otras enfermedades en las que existe alteraciones del tejido conectivo.
Los pacientes portadores de prolapso de válvula mitral, presentan un desplazamiento anormal de una o ambas valvas de la válvula mitral (normalmente la valva posterior) hacia la aurícula izquierda durante la contracción del ventrículo, permitiendo que pequeñas cantidades de sangre fluyan hacia la aurícula, produciendo durante la exploración física que el médico realiza al enfermo lo que se denomina soplo. Esto se debe a que los músculos papilares que sustenta las valvas son demasiados largos e hipertrofiados.
La mayoría de estos pacientes no presentan síntomas pero cuando se produce alguna manifestación los clasificamos en:
- Cardiacas: Dolor en el tórax que se localiza retroesternalmente sobre todo en reposo. Palpitaciones o sensación de que el corazón va a salirse de la caja torácica. Mareo. Síncope. Disnea o falta de aire.
- Extracardiacas: Convulsiones. Hemiparesias. Ambas consecuencia de falta de riego sanguíneo transitorio. Cefaleas. Crisis de ansiedad. Trastorno de pánico. Depresión. Hiperactividad.
4. Complicaciones del prolapso de la válvula mitral
- Insuficiencia mitral, siendo el prolapo de la válvula mitral la principal causa de esta insuficiencia.
- Infección del endocardio.
- Muerte súbita, complicación grave pero muy rara.
5. Exploración física
Como comentamos anteriormente el soplo sistólico constituye el dato más característico a la auscultación. La tensión arterial habitualmente no suele estar alterada. Si bien, es posible observar alteraciones musculoesqueléticas (rectificación de curvas fisiológicas de la columna, pecho en paloma). Como métodos complementarios al diagnóstico se usa el electrocardiograma, ecocardiograma y angiografía.
6. Tratamiento
Si no presenta síntomas, no es necesario realizar nada.
Tratamiento sintomático del dolor torácico.
Si existe insuficiencia mitral se debe realizar una revisión cada 6 o 12 meses, dependiendo del grado de alteración cardiaca que presente el caso. Si la insuficiencia mitral fuese grave y se asociase a alteraciones hemodinámicas estaría indicada la cirugía (sobre todo sustitución valvular).
Profilaxis frente a la infección del encocardio, solo si se evidencia alteración de las valvas (engrosamiento). Y cuando se proceda a: manipulación buco-dental, técnicas sobre el tubo digestivo y vías genitourinarias, y cirugía cardiaca.
Colaboración de :
Federación
Española del Síndrome de X Frágil
www.nova.es/xfragil
A: abreviatura de Adenina
Adenina: Base nitrogenada que forma parte del ADN y del ARN.
ADN: Ácido desoxirribonucleico, se encuentra principalmente formando parte de los cromosomas Es la molécula en
la que está codificada la información genética.
ADNc: Ácido desoxirribonucleico complementario de un ARNm
ADN genómico: ADN que forma parte de los cromosomas.
ADN repetitivo: Secuencia de longitud variable que se repite un número de veces alto en el genoma.
Alelo: Nombre que se le da a dos formas distintas de un mismo gen en los cromosomas homólogos.
Alelos múltiples: Cuando aparecen mas de dos formas de un gen concreto en la población.
Aminoácido: Molécula que posee un grupo carboxilo y uno amino, forma parte de todas las proteínas.
Amniocentesis: Procedimiento usado en el diagnóstico prenatal para obtener amniocitos.
Amniocitos: Células de origen fetal que se encuentran en el liquido amniótico.
Anticipación: Tendencia observable, en algunos tipios de enfermedades en las que los síntomas aparecen mas graves y precoces en generaciones sucesivas.
Autosomas: Cromosomas que aparecen en las células del organismo y son distintos a los sexuales, en los humanos aparecen 22 pares en cada célula somática.
Base nitrogenada: componente de los ácidos nucleicos, en los que aparecen cinco tipos distintos de bases: Adenina, Citosina, Guanina, Timina y Uracilo
Biopsia de vellosidades coriónicas: Procedimiento utilizado en el diagnostico prenatal para obtener una muestra de tejido fetal.
C: Abreviatura de Citosina
Carácter: Característica o rasgo que se observa en un individuo y forma parte de su fenotipo
Célula: Unidades básicas de las que se componen los organismos pluricelulares.
Célula germinal: Aquellas células del organismo que transmiten la información genética a la siguiente generación de individuos.
Cigoto: Óvulo que ha sido fecundado por un espermatozoide.
Citoqenética: Rama de la genética que se ocupa del estudio de los cromosomas.
Citoplasma: Parte de la célula limitada por la membrana externa y la nuclear.
Congénita: Anomalía presente en el individuo a nacer.
Cromosomas: Estructuras filiformes que se observan en los núcleos de las células en el momento de la división celular están formados por ADN y proteínas, en ellos está codificada la información genética que sirve para determinar todas las funciones y formas de las células de un organismo vivo.
Cromosomas sexuales: Par de cromosomas distinto a los pares autosómicos, que están implicados, entre otras funciones, en la determinación del sexo del organismo, en la mujer son dos cromosomas X, y en el varón un X y un Y.
CpG: Región o isla de ADN rica en citosinas y guaninas, regula la transcripción de los genes eucariotas, entre ellos el gen Fmr-1.
Delección: Pérdida de un fragmento cromosómico.
Diagnóstico en la preimplantación: Detección de un trastorno hereditario antes de la implantación, realizada en un cigoto tras una fecundación "in vitro".
Diagnóstico prenatal: Pruebas empleadas para determinar si el feto presenta alguna alteración que e provoque alguna enfermedad.
Dominante: Carácter que se manifiesta siempre en los individuos aunque los dos alelos el gen o genes que lo determinan sean diferentes (heterocigotos).
Dosis génica: Cantidad total de genes de un individuo.
Efecto fundador: Efecto observado en algunas enfermedades genéticas, en las que los individuos afectados en la actualidad, descienden de un antepasado común.
Fenotipo: Características físicas, bioquímicas y fisiológicas de un individuo que resultan de la interacción del genotipo y el entorno.
Fmr-1: Gen del retraso mental ligado al sitio frágil 1, situado en el locus FRAXA.
Fmr-2: Gen del retraso mental ligado a sitio frágil 2, situado en el locus FRAXE.
G: Abreviatura de Guanina, base nitrogenada componente de ADN.
Gameto: Célula germinal del organismo puede ser óvulo o espermatozoide y contiene una sola copia de cada cromosoma (dotación genética haploide).
Gen: Parte de la secuencia del ADN que codifica para una secuencia de aminoácidos en la proteína.
Genoma: Conjunto de todos los genes de una célula.
Genotipo: Constitución genética de un individuo.
Haplotipo: Variantes que se observan en una región cercana, ligada a un gen o alelo concreto, del mismo cromosoma.
Heterocigoto: Individuo que muestra dos alelos distintos en un gen concreto en el par de cromosomas homólogos.
Homocigoto: Individuo que muestra dos alelos idénticos en un gen concreto en el par de cromosomas homólogos.
Inactívación del cromosoma X: Proceso que ocurre en las células femeninas debido a que llevan dos cromosomas X, para compensar la dosis génica respecto a las células masculinas que sólo llevan un cromosoma X.
Inestabilidad cromosómica: Punto de rotura del cromosoma que se asocia a ciertas patologías o a alteraciones en la secuencia de nucleótidos.
In vítro: En el laboratorio (literalmente en cristal).
IQ: coeficiente de inteligencia (valor numérico).
Ligamiento: Se dice que dos genes están ligados cuando están tan cerca en el cromosoma que se observa que se heredan juntos.
Ligamiento al cromosoma X: Genes situados en el cromosoma X
Ligamiento al sexo: Caracteres que se encuentran determinados por genes situados en los cromosomas sexuales X o Y. Locus (Plural Loci): Lugar en el que se sitúa un gen en un cromosoma.
Macroorquidismo: Tamaño de los testículos por encima de la media de la población.
Mosaicísmo: Presencia de distintos caracteres genéticos en los tejidos del organismo.
Mutación: Cambio ocurrido en el material genético que se hereda.
Núcleo: Estructura de las células eucariotas donde se sitúan los cromosomas.
Nucleótido: Unidades básicas del ADN formada por una base nitrogenada, una pentosa y un grupo fosfato, sirven de códigos para los caracteres heredables.
POR: Reacción en cadena de la polimerasa, se consigue amplificar parte del ADN.
Penetración: Proporción de individuos heterocigotos para un carácter en los que se manifiesta aunque sea levemente.
Portador obligado: Individuo que por el análisis de su familia tiene que tener el carácter que se analiza.
Prevalencia: Cálculo de la proporción de individuos con un carácter en una población.
Proteína: Molécula biológica que esta formada por cadenas de aminoácidos, y que determina una función celular.
Síndrome: Conjunto de características o síntomas que aparecen juntos en una patología o enfermedad
"Southern-blot": Detección en los polimorfismos de restricción del ADN por hibridación con sonda marcada.
T: Abreviatura de timina.
Telómero: Parte final de un cromosoma.
Terapia genética: Tratamiento de una enfermedad introduciendo el gen alterado en las células del organismo vivo.
Traducción: Proceso por el que un ARNm es interpretado como una secuencia de aminoácidos de una proteína.
Triplete: Secuencia de tres nucleótidos en la molécula de ADN o en el ARNm y que codifica para un aminoácido concreto en la proteína.
Xq 27.3-28: Bandas finales del brazo largo del cromosoma X.
(El glosario relacionado, ha sido obtenido del libro: Síndrome X Frágil. Edición de bolsillo. Libro publicado para la I Jornada Andaluza del Síndrome X Frágil)
Colaboración de:
Federación
Española de Síndrome de X Frágil
www.nova.es/xfragil
Federación Española Síndrome X Frágil
Apartado de Correos, 42026
28080 – Madrid
Web: http://www.nova.es/xfragil
Email:
Asociación Síndrome X Frágil de Andalucía
C/. Marina 16-18, 3ºC.
21002 Huelva
Teléfono 959 280190
Asociación Síndrome X Frágil de Aragón
Poeta León Felipe, 18 - 2º - 1
50015 - Zaragoza
Teléfono: 976 525 573
Email:
Asociación Síndrome X Frágil de Baleares
Calle de la Rosa, 3
07003 - Palma de Mallorca (Baleares)
Teléfono 971 714906
Email:
Asociación Síndrome X Frágil de Canarias
Málaga, 7 A - 8º B
35016 Las Palmas de Gran Canaria
Teléfono: 928 334157.
Email:
Asociación Síndrome X Frágil de Castilla - León
Cerradilla, 1
47400 – Medina del Campo (Valladolid)
Teléfono: 983-802953
Email:
Asociación Síndrome X Frágil de Cataluña
La Salle de Gràcia
Plaça del Nord, 14
08012 Barcelona
Teléfono y Fax: 93 2170939
Web: http://www.gencat.es/entitats/xfragil.htm
Email:
Asociación Síndrome X Frágil de Extremadura
Avda. Ruta de la Plata, bloque B-1 (Viviendas MOPU)
10001 - Cáceres
Teléfono: 927 230848
Email:
Asociación Síndrome X Frágil de Galicia
Morteiral, 50 - Celas de Peiro
15189 Culleredo (A Coruña)
Teléfono: 981 668275.
Email:
Asociación Síndrome X Frágil de Madrid
Plaza Carballo, 8 – 10º - 3
28029 Madrid
Teléfonos: 91 7398040 - 91 4071142
Web: http://www.ctv.es/USERS/jgab/
http://web.madritel.es/personales/jggabr/home.htm
Email: .
Asociación Síndrome X Frágil de Murcia
Doña Adela 21- 3º A
30530 Cieza (Murcia)
Teléfono y Fax: 968 762912
Web: http://www.ctv.es/USERS/joguar/
Email:
Asociación Síndrome X Frágil de La Rioja
Doctor Múgica, 1 2º E
26002 Logroño
Teléfono: 941 241149
Email:
Asociación Síndrome X Frágil del País Vasco
Apartado de Correos 64
20700 - Zumárraga (Guipúzcoa)
Teléfono: 943 725543
944 602431
Web: http://www.euskalnet.net/axfrav/
Email:
Asociación Síndrome X Frágil de Valencia
Mayor, 42 – puerta 7
46440 – Almusafes (Valencia)
Teléfono: 600 038016
Web: http://www.xfragil.org
Email:
DIRECCIONES DE INTERNET DE ASOCIACIONES DEL SÍNDROME X FRÁGIL EN EL MUNDO
América del Sur
Argentina
Asociación Síndrome X Frágil de Argentina
Web: http://www.advance.com.ar/usuarios/omowen/
Email:
Brasil
Fundación Brasileña del Síndrome X Frágil
Web: http://www.xfragil.com.br
Email:
Asociación Síndrome X Frágil de Brasil
Web: http://www.xfragil.org.br
Email:
Asociación Síndrome X Frágil de Río de Janeiro
Web: http://www.xfragil-rj.com.br
Email:
Asociación Cataraniense del Síndrome X Frágil
Web: http://www.neurogene.floripa.com.br/xfragil
Email:
Chile
Email:
Uruguay
Web: http://www.xfragil.org.uy
Email:
EUROPA
Alemania
Fragíle X Association of Germany
Web: http://www.frax.de/
Email:
Bélgica
Werkgroep Fragiel
Web: http://titan.glo.be/janj/fragiel.htm/
Email:
Francia
Mosaíques Association des X Fragile
Web : http://www.xfragile.org
Email:
Association Nationale du Syndrome X Fragile
Web: http://www.multimania.com/xfralegoeland
Email:
Holanda
Fragiele X Syndrom
Web: http://up.to/fragile_X
Inglaterra
The Fragíle X Society of England
Web: http://www.fragilex.org.uk
Email:
Irlanda
Irish Fragile X Society
Web: http://www.fragilex-ireland.org
Email:
Italia
Italia
Associazione Italiana Sindrome X Fragile
Web: http://www.xfragile.it/
Email: info@fragile@.it
Noruega
Foreningen for Fragilt X-Syndrom
Email:
Portugal
Associaciao Portuguesa da Sindrome do X Fragil
Web: http://www.fragile.org.pt/
Email:
Suecia
Fraxa Sweden
Web: http://www.fragile-x.nu/
Email:
Suiza
Association Suisse du Syndrome de l’ X Fragile
Web: http://www.x-fragil.org/x-fragile.org/
Email:
ESTADOS UNIDOS
FRAXA Research Foundation (EEUU)
Web: http://www.fraxa.org
Email:
National Fragile X Foundation (EEUU)
Web: http://www.nfxf.org.
Email:
The Nothern California Fragile X Association
Web: http://members.aol.com/ncfxa/northern.htm
Email:
The Fragile X Association of Southern California
Web: http://www.fraxsocal.org/
Email:
Conquer Fragile X Foundation
Web: http://www.cfxf.org/
Email:
Fraxa Illinois Chapter
Web: http://www.topsail.com/fraxahome.htm
Email:
Fragile X Alliance Ohio
Web: http://www.fragilexohio.org
Email:
Carolina Fragile X Project
Web: http://www.fpg.unc.edu/~FX
CANADA
Fragile X Research foundation of Canada
Web: http://www.fragile-x.ca
Email:
Fragilex BC British Columbia
Web: http://fragilexbc.tripod.com/fragilexbc/
Email:
Ongwanada Fragile X Resource Center Canada
Email:
AUSTRALIA
Fragile X Association of Australia – New South Wales
Web: http://www.ozemail.com.au/~fraxilex.index.html
Email:
Fragile X Alliance Inc.
Email:
Western Australia Fragile X Support Group
Email:
Queensland Fragile X Association
Email:
ASIA
Arabia Saudí
Email:
Taiwan
Taiwan Fragile X Association
Email:
Turquia
Turkish Fragile X Syndrome Research Association
Email:
- ELECTROFISIOLOGÍA DEL SUEÑO HUMANO NORMAL
- EEG:
- Arquitectura del sueño
- ONTOGENIA DEL SUEÑO
- REGULACIÓN DEL SUEÑO
- Serotonina, Noradrenalina, Dopamina, Acetilcolina, Adenosina, Histamina, Ácido gammaaminobutírico (GABA), Melatonina, Interleucina.
- TRASTORNO DEL SUEÑO
- A) Disomnias:
- Insomnio primario
- Hipersomnia primaria
- Narcolepsia
-
Trastorno del sueño relacionado con la respiración
- Síndrome de apnea obstructiva del sueño
- Síndrome apnea central del sueño
- Síndrome de hipoventilación alveolar
-
Trastorno del ritmo circadiano
- Tipo sueño retrasado
- Tipo jet lag
- Tipo cambios de turno de trabajo
- Tipo no especificado
- Disomnia no especificada
- B) Parasomnias:
- Pesadillas
- Terrores nocturnos
- Sonambulismo
- Parasomnia no especificada
- C) Relacionado con otro trastorno mental
- D) Otros trastornos del sueño:
- Debido a una enfermedad médica
- Crisis epilépticas
- Cefaleas en racimos y migraña paroxística crónica
- Síndrome de deglución anormal relacionado con el sueño
- Asma relacionada con el sueño
- Síntomas cardiovasculares relacionados con el sueño
- Reflujo gastroesofágico relacionado con el
- Hemólisis relacionada con el sueño (hemoglobinuria)
- Trastorno del sueño inducido por sustancias
- Alcohol
- Anfetaminas y estimulantes afines
- Cafeína
- Cocaína
- Opiáceos
- Sedantes, hipnóticos y ansiolíticos
- Otras
- Debido a una enfermedad médica
- A) Disomnias:
- EVALUACIÓN DE LOS TRASTORNOS DEL SUEÑO
- Historia clínica
- Bioquímica de la sangre
- Autorregistros y cuestionarios
- Pruebas electrofisiológicas, EEG:
Concepto
Los antiguos griegos atribuyeron la necesidad de dormir al dios hypnos (sueño), hijo de la Oscuridad y de la Noche, y hermano de la Muerte. El sueño es un estado fisiológico, activo y rítmico, que aparece cada 24 horas en alternancia con el otro estado de conciencia básico que es la vigilia. Actualmente se admite el sueño como el más importante ritmo circadiano, no sólo porque ocupa la tercera parte de nuestra vida, sino porque afecta a la mayoría de los procesos fisiológicos y psicológicos y, a su vez, es afectado por ellos .
Definiciones relacionadas con el sueño (adaptado de Amercan Sleep Disorders Association Diagnostic, 1990)
| Apnea | Cese del flujo respiratorio durante un periodo superior a 10 seg. |
| Cataplejía | Pérdida súbita del tono muscular, generalmente precipitada por una respuesta emocional. |
| Cronobiología | Estudio de los ritmos fisiológicos naturales. |
| Diurno | Variable conductual o fisiológica relacionada con el día. |
| Hipersomnia | Somnolencia excesiva. Propensión a quedarse dormido. |
| Hipopnea | Reducción del flujo aéreo mayor del 50% y de duración mayor a 10 seg. |
| Insomnio | Dificultad para iniciar o mantener el sueño. |
| Mioclono | Contracción brusca de un grupo muscular. |
| Parasomnia | Suceso conductual o fisiológico adverso que ocurre durante el sueño. |
| Polisomnograma | Registro electrofisiológico durante el sueño. |
| Ritmo circadiano | Patrón regular de fluctuación en la fisiología o en la conducta de 24 horas de duración. |
| Sueño paradójico | Sinónimo de sueño REM o MOR (movimientos oculares rápidos) |
| Zeitgeber | Factor ambiental que ayuda a coordinar los ritmos biológicos. |
Los ritmos circadianos (del latín circa o alrededor y dies o día), tienen varias características:
1. Sincronización con los ciclos ambientales (siendo a nivel ambiental el más importante el ciclo luz-oscuridad).
2. Existen muchos relojes internos que funcionan independientemente, pero de forma sincronizada (en ausencia de ciclos ambientales, los marcapasos circadianos funcionan libremente y expresan su periodicidad endógena, genéticamente determinada.
3. Compensación de la temperatura (mantenimiento del periodo circadiano independientemente de oscilaciones grandes de temperatura).
El sueño lejos de ser un estado de inactividad en donde quedamos reposando en silencio, constituye un estado de gran actividad, donde se operan cambios hormonales, metabólicos, térmicos, bioquímicos y en la actividad mental en general, fundamentales para lograr un equilibrio psicofísico adecuado y un correcto funcionamiento durante el día. Aunque no conozcamos con total exactitud la función del sueño en el humano, no hay duda que la calidad del sueño influye directamente sobre la calidad de nuestra vida.
Actualmente se estudia en los Centros especializados o Laboratorios de Sueño, en los que se realizan las polisomnografías, registros durante una noche completa, donde se realiza la toma de:
1. Electroencefalografía (EEG) pudiéndose hacer con 2 o hasta 32 electrodos cefálicos.
2. Electrooculograma (EOG), dos canales para ver los movimientos oculares.
3. Electromiograma mentoniano (EMG), dos canales, para ver el descenso del tono muscular, inhibido en el REM.
4. Electrodos de referencia. Electrodos en los lóbulos de las orejas.
5. Flujo aéreo buco-nasal. Se coloca un termistor que determinará el flujo de aire.
6. Esfuerzo respiratorio. Cinturón torácico-abdominal que registra el esfuerzo respiratorio.
7. Electrocardiograma (ECG). Dos electrodos subclaviculares para detectar arritmias cardiacas durante el sueño.
8. Electromiograma en extremidades. Electrodos sobre ambos tíbiales anteriores, para determinar movimientos periódicos de piernas, distonías.
9. Sensor de posición. Saber la posición en que esta durmiendo el paciente es importante para el estudio de las apneas.
10. Micrófono. Se coloca en el cuello para registrar ronquidos, somniloquias.
11. Oximetría digital. Informan sobre la saturación de oxígeno asociada o no a las apneas.
12. Vídeo digital. Permite correlacionar movimientos y convulsiones con la aparición de cambios en el trazado electroencefalográfico.
En el trazado electroencefalográfico (EEG), se estudia fundamentalmente la frecuencia o el número de ondas por segundo (medida en herzios), su amplitud (potencial en microvoltios) y su distribución topográfica según las diferentes áreas del cerebrales. Los cuatro ritmos fundamentales que son:
Delta: de frecuencia < 4 Hz, su amplitud es > 5mV, y se recoge en todas las regiones cerebrales. Se produce en las fases más profendas de sueño
Theta: entre 4 y 8 Hz, baja amplitud, y en regiones temporales.
Alfa: de frecuencia 8 - 13 Hz (la frecuencia dominante en el adulto), su amplitud < 50 mV, en regiones posteriores del encéfalo. Se produce en estado de relajación o vigilia tranquila.
Beta: que varía entre los 12 y los 30 Hz, su amplitud < 30 mV, en regiones frontales y centrales del encéfalo. Se recoge en estado de vigilia y en diversas fases del sueño.
También se utiliza el EEG como Test Repetido de Vigilia Sostenida (RTSW = repeated test of sustained wakefulness). Se coloca al individuo en una habitación sin ruidos y con poca iluminación, y se le indica que permanezca despierto; este procedimiento se repite varias veces durante el día. Las medidas del sueño comprenden:
La continuidad del sueño se define como el promedio total de sueño y vigilia durante una noche. Una continuidad de sueño indica un sueño consolidado y con pocos despertares.
Latencia del sueño: el tiempo requerido para dormirse (expresado en minutos)
Despertares intermitentes: el tiempo que se permanece despierto, una vez iniciado el sueño (expresado en minutos)
Eficacia del sueño: el cociente entre el tiempo dormido y el tiempo permanecido en cama (expresada en porcentaje, las cifras elevadas indican una mejor continuidad del sueño).
Mediante la polisomnografía se pueden registrar tres estados de actividad y función: vigilia, sueño con movimientos oculares rápidos (REM o MOR), y sueño con reducción de los movimientos oculares rápidos (sueño NREM o NMOR). El sueño REM, descubierto en 1953 por Aserinsky y Kleitman, es un estado fisiológico durante el cual el cerebro se activa eléctricamente y metabólicamente, con frecuencias similares al estado de vigilia y acompañado por un aumento entre el 62 y el 173% del flujo sanguíneo cerebral. Quizás como defensa para conservar el sueño, existe una atonía muscular generalizada que se detecta polisomnográficamente por la desaparición de la actividad electromiográfica. Los movimientos rápidos de los ojos se producen en forma de una secuencia de salvas acompañada por fluctuaciones en el ritmo cardíaco y respiratorio. Se observa una ingurgitación peneana y clitoridiana, seguramente debida a un aumento del tono colinérgico asociado con el estado REM. Asimismo se observa una supresión de la regulación térmica normal, por lo cual los seres humanos se convierten de forma temporal en seres poiquilotérmicos. Finalmente, el sueño REM es el estadio en el que se producen los sueños más vívidos y en ocasiones más extraños. El sueño reparador en los humanos se compone de ciclos recurrentes de 70 a 120 minutos de sueño NREM y sueño REM, que se caracterizan polisomnográficamente mediante el electroencefalograma (EEG), electrooculograma (EOG) y el electromiograma (EMG) Los movimientos oculares son detectados mediante el EOG debido a la existencia de un dipolo eléctrico entre la córnea y la retina.
Habitualmente, el sueño progresa desde la vigilia, a través de las cuatro etapas de sueño NREM, hasta el inicio del primer período REM. En un adulto sano, los estadios más profundos del sueño, los estadios 3 y 4 del sueño NREM (a los que nos referimos como sueño de ondas lentas), se producen en los dos primeros períodos NREM. En contraste, los períodos REM durante la primera mitad del sueño son breves, aumentando su duración a medida que se van sucediendo ciclos. Durante la vigilia, el EEG se caracteriza por una rápida actividad de bajo voltaje que consiste en una mezcla de frecuencias alfa (8 a 13 Hz) y beta (>13Hz). El estadio 1 del sueño NREM es un estado transicional entre la vigilia y el sueño en el cual desaparece el ritmo alfa predominante y aparecen frecuencias theta (4 a 7 Hz) más lentas. La actividad electromiográfica disminuye y los ojos se mueven de forma oscilante y lenta. El estadio 2 se caracteriza por un ritmo theta de fondo y la aparición episódica de puntas del sueño (breves trenes de pulsos de actividad con una frecuencia entre 12 y 14 Hz) y de complejos K (onda electronegativa de baja frecuencia y elevada amplitud seguida de una onda electropositiva). El tono muscular continúa disminuido y los movimientos oculares son esporádicos. Los estadios 3 y 4 se definen como períodos del sueño constituidos por actividad de gran amplitud en la banda delta (0,5 a 3,0 Hz) en más del 20 y del 50% de la duración del estadio, respectivamente. Los músculos están casi atónicos y no se observan movimientos oculares. El sueño REM se caracteriza por un EEG con frecuencias mixtas y de baja amplitud, movimientos rápidos de los ojos y ausencia de tono muscular.
El sueño experimenta importantes cambios a lo largo del ciclo vital en el ser humano, que se refieren a su duración total, a su distribución en las 24 horas y a su composición estructural.
El tiempo diario de sueño en el recién nacido es de hasta 20 horas diarias, que disminuyen de forma lenta a 13-14 a los 6-8 meses. Desde el tercer mes existe un patrón circadiano establecido. A los 2 años la duración nocturna es de 12 horas, hacia los 10 años de 10 y en el adulto joven de 8, con amplias variaciones entre distintos individuos. Al comienzo de la vida los niños pasan directamente de vigilia a sueño REM, y desde el tercer mes de vida, el sueño comienza con sueño NREM. Hacia el primer año se consolida una clara diferenciación de las fases del sueño NREM, a la vez que se estabiliza la duración del sueño REM, alrededor del 25% del tiempo dormido cada día, todo ello debido a la relativa inbmadurez de las estructuras nerviosas que controlan el sueño.
Hacia los 6 años, se configura de forma estable la duración de los ciclos del sueño en unos 105-110 minutos, se caracteriza por elevados porcentajes de sueño MOR y sueño de ondas lentas de elevada amplitud. Durante la adolescencia se produce una disminución importante del sueño d ondas lentas.
De la tercera a la sexta década de la vida se produce una disminución lenta y gradual de la eficacia del sueño y del tiempo total de éste. A medida que avanza la edad, el sueño se vuelve más fragmentado y ligero. El sueño se modifica con la edad no solo en su cantidad (disminución total de sueño nocturno) sino también en su estructura (fragmentación del sueño con aumento del número de despertares nocturnos, con importante disminución del sueño profundo y menor disminución del sueño REM que además se desplaza alas primeras horas del dormir) y también se modifica su distribución temporal: el ritmo vigilia-sueño vuelve a ser polifásico y se produce un avance progresivo de fase (se acuestan antes y se levantan antes).
En los mayores de 65 años tiene lugar una mayor prevalencia de alteraciones del sueño (entre 25 y 50%), en gran medida secundarias o sintomáticas de trastornos médicos o psiquiátricos, por lo que resulta fundamental tenerlos en cuenta para llevar a cabo su tratamiento. El sueño pierde calidad y se altera al aumentar la edad, es más superficial, a la vez que aumenta la latencia del sueño y disminuye el tiempo total, aunque no es por la edad en sí misma sino por el grado relativo de salud personal. El deterioro de la calidad del sueño es paralelo al daño estructural y a la disfunción del SNC como puede medirse a través del funcionamiento cognitivo y del flujo sanguíneo cerebral. A medida que aumenta la edad, se produce un acortamiento del ritmo circadiano endógeno subyacente con tendencia a despertarse más temprano de forma progresiva (Buysse y cols., 1992).
El desarrollo del sueño normal es proceso dinámico que se ve modificado (en su relación sueño REM/NREM) desde el feto al anciano, donde en el recién nacido el 50% del sueño está constituido por sueño REM, y alrededor del cuarto mes de vida el ciclo del sueño comienza a mostrar un patrón similar al del adulto y la latencia del REM se hace cada vez más prolongada. La proporción del sueño REM va disminuyendo hasta que entre los 3-5 años ocupa solo el 20 % del dormir, permaneciendo esta proporción durante la vida adulta. El sueño lento profundo, en las etapas 3-4 disminuye paulatinamente a partir de los 20 años y usualmente desaparece a partir de los 60 años de edad, y esta disminución del sueño lento se diferencia según el sexo, manteniéndose en las mujeres hasta edades más avanzadas. También la distribución de las horas durante el día van variando según la edad, siendo con un patrón polifásico en el recién nacido y en el anciano, mientras desde los 4 años hasta los 60 años aproximadamente es monofásico. El sueño REM en cambio se mantiene constante aún en los ancianos y este esta relacionado con la función intelectual, observándose una declinación muy marcada en los pacientes con demencia.
En la actualidad, la idea que prevalece es que no existe un único centro del SNC que controle el sueño, sino que existe un número de sistemas o centros interconectados, que se activan mutuamente o se inhiben unos a otros, a través de los neurotransmisores y neuromoduladores, los principales son:
Serotonina
Muchos estudios apoyan la participación de la serotonina (5-HT) en el sueño, ya que la administración del L-triptófano induce al sueño y se le llama hipnótico natural. La síntesis y liberación de serotonina dependen de la disponibilidad de aminoácidos precursores del L-triptófano (de 1 a 15g), que reduce la latencia de sueño y los despertares nocturnos. Por el contrario, la deficiencia de L-triptófano se asocia a una reducción del sueño MOR. Sin embargo no se utiliza a nivel clínico, porque se le relacionó con el síndrome de mialgia eosinofílica.
Lesiones en el núcleo dorsal del rafe se acompañan de agotamiento de la serotonina e insomnio que dura días. La administración de p-clorofenilalanina inhibe a la hidrosilasa de triptófano y también produce insomnio en el gato durante 3 o 4 días. Este insomnio puede revertirse con la administración de 5-hidroxitriptófano, otro precursor de la serotonina que evita el sitio de inhibición enzimática de la p-clorofenilalanina. Por otro lado, la serotonina regula la aparición de espigas ponto-geniculo-occipitales (PGO), las cuales aparecen segundos antes del inicio del sueño NMOR y durante todo el tiempo que dura éste.
Los niveles de serotonina varían a lo largo del día, así como el número y afinidad de sus receptores. Los 5-HT tienen niveles máximos durante el día y disminuye durante la noche; los receptores muestran una curva inversa, ya que son más abundantes y afines durante la noche. En experimentos de deprivación de sueño se detectó aumento de los niveles de serotonina, pero los receptores no se modificaban.
Noradrenalina
En un estado de activación intervienen dos áreas cerebrales, cada una con un neurotransmisor propio, son el locus coeruleus y la sustancia negra. Las neuronas que contienen noradrenalina, cuyos cuerpos celulares se localizan en el locus coeruleus, están muy activas durante la vigilia, pero se encuentran silentes durante el sueño MOR. Las lesiones en esta área producen hipersomnia (exceso de sueño), aumentando tanto el sueño de ondas lentas como el sueño MOR (Jones, Bobillier y Jouvet, 1969). En seres humanos, la estimulación eléctrica del locus coeruleus, altera profundamente todos los parámetros del sueño.
Los estudios farmacológicos ofrecen resultados contradictorios. La inhibición de la hidrosilasa de tirosina con alfa-metil-paratoroxina (AMPT), produce un descenso de la noradrenalina y la dopamina con hipersomnia y disminución de la latencia hasta el NMOR. Estudios posteriores que analizaron el papel de los receptores alfa1, alfa2 y adrenérgicos-b, mostraron que hay una interacción importante entre ellos en el mantenimiento y equilibrio del ciclo sueño-vigilia. La administración periférica de clonidina, un agonista alfa2 que disminuye la liberación de noradrenalina, disminuye el sueño NMOR y MOR; la aplicación local de clonidina en el locus coeruleus suprime el NMOR. El empleo de un antagonista alfa1 como la fenoxibenzamina también reduce el NMOR. También es probable que la noradrenalina participe en la aparición del ritmo theta, ya que la administración de clonidina y p-aminoclonidina induce la actividad theta hipocámpica. En general, los agentes que aumentan la disponibilidad de la noradrenalina en la hendidura sináptica suprimen el NMOR, no obstante, hay excepciones como la clonidina, la cual disminuye la liberación de este neurotransmisor y también suprime el MOR.
Dopamina
El segundo sistema de activación se localiza en la sustancia negra, cuyas neuronas utilizan un neurotransmisor catecolaminérgico, la dopamina. Este centro está implicado en la coordinación motora y en el tono muscular postural. Los efectos de las anfetaminas y la cocaína sugieren el papel este neurotransmisor en el mantenimiento de la vigilia. Las anfetaminas son estimulantes que aumentan la vigilia y disminuyen el NMOR. Los efectos de las anfetaminas pueden bloquearse con pimocida, un antagonista que se utiliza como neuroléptico en la práctica clínica.
Los niveles de dopamina son altos durante la vigilia y el recambio disminuye en la transición del estado de despierto a dormido. En estudios animales, la apomorfina (un antagonista dopaminérgico), origina un predomino de la vigilia a expensas del sueño, sobre todo del NMOR. Se obtiene el efecto contrario con la administración de pimocida y otros neurolépticos (sulpiride y haloperidol) antagonistas de los receptores dopaminérgicos D2.
En general, las sustancias que incrementan la dopamina cerebral producen activación y vigilia, por el contrario los bloqueadores de la dopamina como la pimocida y las fenotiacidas, tienden a incrementar el tiempo de sueño.
Acetilcolina
La acetilcolina cerebral también está implicada en la regulación del sueño, en particular en la producción del MOR. En humanos, los agentes agonistas colinérgicos como la fisostigmina, arecolina, RS-86 y pilocarpina inducen el NMOR; por el contrario la escopolamina, un antagonista no selectivo y el biperidén selectivo para los receptores muscarínicos M1, tienen efectos opuestos.
Parece que un grupo de neuronas colinérgicas en la formación reticular de la protuberancia se encargan del inicio y mantenimiento del NMOR. La administración sistemática de atropina produce ondas lentas de gran amplitud, mientras que la infusión local de agonistas en la formación reticular aumenta la desincronización cortical y la intensidad del despertar conductual.
La actividad theta es uno de los componentes tónicos del NMOR, el sistema colinérgico es un mediador parcial de éste, de manera que la atropina puede modificar elementos de la actividad theta. La atonía también tiene componente colinérgico, ya que la inhibición de los músculos antigravitatorios proviene de la activación de grupos de neuronas no aminérgicas que se localizan en la periferia del locus coeruleus (peri-LC-alfa). La infusión de carbacol dentro del tegmento pontino induce cataplexia rápida en el gato.
También se asocia la acetilcolina (Ach) con la actividad PGO. La administración de atropina reduce significativamente los trenes de estas espigas, sin embargo también neuronas naradrenérgicas y serotoninérgicas tienen influencia inhibitoria sobre las espigas PGO. La administración de reserpina, que bloquea el almacenamiento de monoaminas e índoles, da lugar a la aparición de PGO en vigilia y en otras fases de sueño diferentes a la de MOR.
Las alteraciones en la actividad colinérgica central se asocian a cambios de sueño observados en el Trastorno Depresivo Mayor, que muestran anormalidades importantes en los patrones del MOR, entre ellas: acortamiento de la latencia MOR (60´), incremento del porcentaje de sueño MOR, y un cambio en la distribución del mismo desde la primera mitad de la noche hasta la última. La administración de un agonista muscarínico, a pacientes deprimidos durante el primer o segundo periodo NMOR provoca un rápido inicio del sueño MOR. Así, la depresión puede asociarse a una hipersensibilidad subyacente a la acetilcolina (Kaplan y cpls., 1996).
Las sustancias que reducen el sueño MOR, como los antidepresivos, producen efectos beneficiosos sobre la depresión, además casi la mitad de los pacientes con un trastorno depresivo mayor experimentan mejorías temporales cuando se les depriva del sueño. Por el contrario, la reserpina, que es una de las pocas sustancias que aumentan el sueño MOR, también produce depresión.
Los pacientes con Demencia tipo Alzheimer presentan alteraciones en el sueño caracterizadas por una reducción del MOR y sueño de ondas lentas. La pérdida de neuronas colinérgicas en el cerebro anterior se implican en estos cambios.
Adenosina
La adenosina es un nucleósido de purina tiene efectos sedantes e inhibitorios sobre la actividad neuronal. La cafeína disminuye el sueño precisamente por el bloqueo del receptor de adenosina. La adenosina aumenta el sueño NMOR (sobre todo en el estadio IV) y también el NMOR. Cuando se aplica un inhibidor de la desaminasa de adenosina (desoxicoformicina) se incrementa el NMOR. Se observó el mismo efecto con el precursor de la adenosina, el S-adenosil homocisteína.
Aún no se identifica el papel de la adenosina en la vigilia, pues los receptores de adenosina A1 tras la privación de NMOR estaban elevados, sin embargo los niveles de adenosina a las 48 horas de abstinencia no estaban altos.
Histamina
El papel de la histamina en el ciclo vigilia-sueño se identificó en base a observaciones farmacológicas en el mantenimiento de la vigilia y del efecto sedante de los antagonistas de los receptores H1, que en los humanos producen somnolencia. Estos antihistamínicos acortan la latencia del sueño, pero no modifican significativamente el sueño nocturno, por ello es un componente frecuente en los inductores al sueño. El principal problema es que crea una tolerancia rápida al efecto hipnótico. Los medicamentos que actúan sobre los receptores H2 no parecen tener efecto sobre la vigilia, pero aumentan la cantidad de sueño delta.
Se supone que hay una vía histaminérgica ascendente que proporciona inervación a la corteza, cuerpo estriado, hipocampo y amígdala, cuyos cuerpos celulares se localizan en el hipotálamo posterior y regiones difusas del mesencéfalo, que en el hombre, participarían del control de la vigilia y en el equilibrio entre vigilia y sueño.
GABA
La principal evidencia que relaciona al Ácido gammaaminobutírico (GABA) con los mecanismos del sueño son las asociaciones entre los receptores gabaérgicos y las benzodiacepinas, que hoy día son los medicamentos hipnóticos de mayor prescripción. La administración de l-cicloserina inhibe la destrucción del GABA, y tiene un efecto similar al de las benzodiacepinas en el sueño, con la diferencia que las dosis bajas no suprimen el NMOR. Es muy probable que el efecto del GABA sobre el sueño sea indirecto, a través de los otros neurotransmisores que tienen una actividad más específica.
Melatonina
La melatonina es la principal hormona de la glándula pineal. Su precursor primario es la serotonina, cuya concentración en la glándula pineal durante el periodo luminoso es superior a la de cualquier estructura del SNC. El nivel máximo de actividad de sus enzimas sintéticas se alcanza durante la oscuridad, por lo tanto el periodo de mayor secreción es por la noche. Es decir, la secreción de melatonina desde la glándula pineal queda inhibida por la luz brillante, por lo tanto la menor concentración de melatonina sérica se observa durante el día.
Se informa que la melatonina aumenta el sueño delta; la administración de 50mg intravenosa acorta la latencia hasta el sueño, mientras que 80mg por vía oral aumenta la somnolencia. A dosis menores se refiere un aumento de latencia a NMOR. La privación de sueño demuestra un aumento de la amplitud de secreción de melatonina, sin cambios de cortisol. La administración contínua de melatonina (2mg) en la tarde originó cansancio excesivo y aumento en la concentración plasmática que excedió entre 10 y 100 veces la concentración fisiológica nocturna.
En el hombre, la melatonina se ha estudiado en relación al síndrome afectivo estacional, conocido como depresión estacional o invernal, donde se refieren bajos niveles de melatonina. Ello se debe a que las terminales nerviosas que activan a los pinealocitos son noradrenérgicas y si en la depresión hay bajo nivel de este NT, explica la baja producción de melatonina Uno de los tratamientos utilizados es el aumento de luz artificial o fototerapia.
Interleucina
Se supone una relación entre el sueño y el sistema inmunitario. En el humano, se ha encontrado que la interleucina 1 (IL-1) sérica se eleva en el sueño, y sabemos que ésta se libera a partir de los macrófagos para activar a los linfocitos T e induce la fiebre por su acción sobre las células hipotalámicas. En animales la IL-1 incrementan el sueño NMOR en forma dependiente de la dosis. También previene el aumento de temperatura cuando se administra por vía intravenosa, lo cual no impide el efecto somnogénico. En el hombre se detecta un pico de IL-1, durante la primera etapa de ondas lentas de inicio del sueño.
Los trastornos primarios del sueño son aquellos que no tienen como etiología ninguno de los siguientes trastornos: otra enfermedad mental, una enfermedad médica o el consumo de una sustancia. Estos trastornos del sueño aparecen presumiblemente como consecuencia de alteraciones endógenas en los mecanismos del ciclo sueño-vigilia, que a menudo se ven agravadas por factores de condicionamiento. Los trastornos del sueño están divididos en cuatro grandes apartados según su posible etiología .
Clasificación de los Trastornos del Sueño (DSM-IV-TR)
TRASTORNOS PRIMARIOS DEL SUEÑO
A) DISOMNIAS
Insomnio primarioHipersomnia primariaNarcolepsiaTrastorno del sueño relacionado con la respiraciónTrastorno del ritmo circadiano (trastorno del ritmo sueño-vigilia)Tipo sueño retrasadoTipo jet lagTipo cambios de turno de trabajoTipo no especificadoDisomnia no especificada
B) PARASOMNIAS
Pesadillas (Trastornos por sueños angustiosos)Terrores nocturnosSonambulismoParasomnia no especificada
C) TRASTORNOS DEL SUEÑO RELACIONADOS CON OTRO TRASTORNO MENTAL
Insomnio relacionado con otro trastorno mental (Eje I o Eje II)Hipersomnia relacionada con otro trastorno mental (Eje I o Eje II)
D) OTROS TRASTORNOS DEL SUEÑO
Trastorno del sueño debido a una enfermedad médicaTipo insomnioTipo hipersomniaTipo parasomniaTipo mixtoTrastorno del sueño inducido por sustanciasTipo insomnioTipo hipersomniaTipo parasomniatipo mixto
Son trastornos primarios del inicio o el mantenimiento del sueño, o de somnolencia excesiva, que se caracterizan por un trastorno de la cantidad, la calidad y el horario del sueño. Incluye el insomnio primario, la hipersomnia primaria, la narcolepsia, el trastorno del sueño relacionado con la respiración, el trastorno del ritmo circadiano y la disomnia no especificada.
Los individuos con insomnio primario presentan muy a menudo una combinación de dificultades para dormir y despertares frecuentes durante la noche. Con menos frecuencia se quejan únicamente de no tener un sueño reparador, es decir, tienen la sensación de que su sueño ha sido inquieto, poco profundo y de poca calidad. Este trastorno se suele asociar con un aumento del nivel de alerta fisiológica y psicológica durante la noche, junto a un condicionamiento negativo para dormir.
La preocupación intensa y el malestar por la imposibilidad de dormir bien pueden generar un círculo vicioso: cuanto más intenta el individuo dormir, más frustrado y molesto se encuentra, y menos duerme. Estar acostado en una cama en la que la persona ha pasado a menudo noches sin dormir puede producir frustración y activación condicionada. Por el contrario, el individuo puede dormirse más fácilmente cuando no lo intenta (mientras mira la televisión, lee o conduce el coche). Algunas personas con un estado de alerta alto y un acondicionamiento negativo explican que duermen mejor fuera de su dormitorio y de su entorno. El insomnio crónico puede provocar una disminución de la sensación de bienestar durante el día (alteración del estado de ánimo y de la motivación; atención, energía y concentración disminuidas, y un aumento de la sensación de fatiga y malestar).
La característica esencial de la hipersomnia primaria es una somnolencia excesiva durante al menos 1 mes, evidenciada tanto por episodios prolongados de sueño como por episodios de sueño diurno que se producen prácticamente cada día. La somnolencia excesiva debe ser de suficiente gravedad como para provocar malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo; no aparece exclusivamente en el transcurso de otro trastorno del sueño o de otro trastorno mental, ni se debe a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
En los individuos con hipersomnia primaria la duración del episodio de sueño más largo (para la mayoría de las personas, el sueño nocturno) oscila entre 8 y 12 horas, y a menudo se acompaña de problemas a la hora de levantarse. La calidad real del sueño nocturno es normal. La somnolencia excesiva durante las horas habituales de vigilia toma la forma de siestas intencionadas o de episodios de sueño inadvertidos. Las determinaciones objetivas demuestran una somnolencia fisiológica aumentada. Las siestas durante el día tienden a ser relativamente largas, el individuo no nota que sean reparadoras y no producen una mejora en el nivel de alerta. Habitualmente, las personas que padecen este trastorno presentan la somnolencia de forma creciente a lo largo de un período de tiempo determinado, no experimentando «ataques» repentinos de sueño. Los episodios de sueño no intencionados tienen lugar habitualmente en situaciones de baja estimulación y baja actividad como durante conferencias, leyendo, mirando la televisión o conduciendo.
La hipersomnia puede provocar malestar significativo y deterioro social y laboral. El sueño nocturno prolongado y la dificultad para levantarse pueden producir problemas a la hora de cumplir con las obligaciones laborales. Los episodios no intencionados de sueño durante el día son a veces muy molestos e incluso peligrosos si, por ejemplo, el individuo está conduciendo o trabajando con una máquina. El nivel de alerta disminuido que se observa cuando el sujeto intenta combatir la somnolencia puede comportar un bajo rendimiento, una pobre concentración y un déficit de memoria durante las actividades diurnas.
La mayoría de los individuos con hipersomnia primaria tienen síntomas persistentes y de importancia. En la forma recidivante de la hipersomnia primaria, conocida como síndrome de Kleine-Levin, los individuos pueden llegar a pasar 18-20 horas durmiendo o en la cama. Los episodios recidivantes de somnolencia se asocian a otras características clínicas de desinhibición: hipersexualidad indiscriminada, episodios de ingesta excesiva y compulsiva, con ganancia de peso y en algunos individuos se han descrito irritabilidad, despersonalización, depresión, confusión y alucinaciones ocasionales, así como comportamientos impulsivos.
La característica esencial de la narcolepsia es la aparición recurrente e irresistible de sueño reparador, cataplejía e intrusiones recurrentes de elementos característicos de la fase REM en el período de transición entre el sueño y la vigilia. La somnolencia del individuo disminuye típicamente tras el ataque de sueño y sólo reaparece varias horas después. Los ataques de sueño han de ocurrir diariamente en un período de al menos 3 meses para poder establecer el diagnóstico aunque la mayoría de los individuos manifiesta haber padecido ataques de sueño durante muchos años antes de solicitar ayuda terapéutica. Además de somnolencia, los individuos con narcolepsia experimentan uno o ambos de los siguientes síntomas: cataplejía (es decir, episodios súbitos de pérdida bilateral del tono muscular que duran entre segundos y minutos y que suelen estar desencadenados por emociones intensas) o intrusiones recurrentes de elementos característicos de la fase REM en el período de transición que va del sueño a la vigilia y que se traducen en parálisis de los músculos voluntarios o alucinaciones de carácter onírico. Los síntomas no se deben a los efectos fisiológicos directos de una sustancia (incluyendo fármacos) o de otra enfermedad médica. Los episodios de somnolencia de la narcolepsia suelen describirse como irresistibles, dando lugar a sueño de carácter involuntario en situaciones claramente inadecuadas como puede ser al mantener una conversación. Las situaciones poco estimulantes o poco activas exacerban típicamente el grado de somnolencia.
Los episodios de sueño suelen durar 10 a 20 minutos, pudiendo llegar a horas si no se ven interrumpidos. Es frecuente que estos individuos relaten actividad onírica durante tales episodios. Las personas que padecen narcolepsia disponen de diversas estrategias para «neutralizar» estos ataques de sueño. Cuando no se sigue tratamiento, el número de episodios diarios de sueño (intencionado o no intencionado) se sitúa entre 2 y 6. Los episodios de sueño suelen aparecer sobre un nivel de alerta relativamente normal, aunque algunos individuos confiesan presentar de forma constante algún grado de somnolencia. La cataplejía acostumbra a aparecer varios años después de establecida la somnolencia diurna e incide aproximadamente en un 70 % de los individuos que sufren el trastorno. En la cataplejía la pérdida del tono muscular debe ser de carácter brusco, dando lugar a una caída de la mandíbula, la cabeza o los brazos, no observable por los demás. A veces la cataplejía reviste un carácter mucho más espectacular, y así, al individuo pueden caérsele objetos que esté transportando, puede desplomarse sobre sus rodillas o caerse realmente al suelo. La musculatura respiratoria y ocular está respetada. La debilidad muscular suele durar sólo unos segundos, aunque se han descrito episodios de hasta media hora de duración. La recuperación de la fuerza muscular es total e inmediata. Durante los episodios estos individuos conservan la conciencia y el estado de alerta, de forma que son capaces de describir perfectamente y sin confusión todo lo que ha ocurrido en ese momento. Aunque no es frecuente, los ataques prolongados de cataplejía pueden desembocar en episodios de sueño. La cataplejía suele estar desencadenada por estímulos emocionales intensos. La deprivación del sueño aumenta la frecuencia y la intensidad de los episodios de cataplejía. Aproximadamente el 20-40 % de los individuos con narcolepsia presenta asimismo imágenes que recuerdan mucho los sueños justo antes de quedarse dormidos (alucinaciones hipnagógicas) o justo después de despertarse (alucinaciones hipnopómpicas). La mayor parte de las alucinaciones relacionadas con el sueño son de carácter visual e incorporan elementos del entorno real. Las alucinaciones también son de carácter auditivo o cinético. Aproximadamente el 30-50 % de los individuos con narcolepsia experimenta asimismo parálisis del sueño justo en el preciso momento de dormirse o despertarse. En este trastorno los individuos describen estar despiertos, pero son incapaces de moverse o hablar. También pueden aquejar incapacidad para respirar; lo cierto es que el diafragma deja de trabajar, si bien la respiración no se detiene. Las alucinaciones relacionadas con el sueño y las parálisis del sueño aparecen a veces de forma simultánea, lo que lugar a una experiencia terrorífica de ver y/o escuchar cosas inusuales sin poder escapar, pudiendo durar entre segundos a minutos.
En aproximadamente un 40 % de los individuos con narcolepsia se detecta un trastorno mental actual o pasado. Entre los trastornos asociados más a menudo se encuentran los trastornos del estado de ánimo (especialmente el trastorno depresivo mayor y la distimia), seguidos de los trastornos relacionados con sustancias y el trastorno de ansiedad generalizada. También presentan una mayor incidencia de antecedentes de parasomnias como sonambulismo, bruxismo (cierre de la mandíbula y rechinar de los dientes), y enuresis.
La característica esencial de este trastorno es una desestructuración del sueño que da lugar a somnolencia excesiva o insomnio, y que se considera secundaria a alteraciones de la ventilación durante el sueño (p. ej. , apnea del sueño o hipoventilación alveolar central). La somnolencia excesiva constituye el motivo de consulta más frecuente de los individuos con trastorno del sueño relacionado con la respiración. Esta somnolencia está producida por los frecuentes aumentos de activación que lleva a cabo el individuo durante el sueño nocturno en un intento por respirar de forma normal. La somnolencia se hace más patente en situaciones de relajación como leer o ver la televisión. La incapacidad del individuo para controlar esta somnolencia puede hacerse evidente revistiendo un carácter extremo, y la persona puede quedarse dormida incluso en situaciones activas como hablar, comer, andar o conducir.
Algunos individuos aquejan dificultad para respirar en posición supina o al dormir. Entre las alteraciones respiratorias que tienen lugar durante el sueño en este trastorno se incluyen las apneas que son episodios de interrupción de la respiración, hipoapneas (respiración anormalmente lenta o superficial) e hipoventilación (niveles sanguíneos de oxígeno y dióxido de carbono anormales). Se han descrito tres formas de trastorno del sueño relacionado con la respiración:
Es la forma más frecuente de trastorno del sueño relacionado con la respiración. Se caracteriza por episodios repetidos de obstrucción de las vías aéreas superiores (apneas o hipoapneas) durante el sueño. Los impulsos nerviosos que rigen los movimientos respiratorios en el tórax y el abdomen están preservados. Esta forma del trastorno del sueño relacionado con la respiración suele incidir en individuos con sobrepeso y conducir a un estado de somnolencia excesiva. El síndrome de apnea obstructiva del sueño se caracteriza por ronquidos intensos o inspiraciones bruscas breves que alternan con episodios de silencio respiratorio que suelen durar 20-30 seg. Los ronquidos obedecen al paso de aire por unas vías aéreas parcialmente obstruidas. Los períodos de silencio respiratorio traducen las propias apneas obstructivas, es decir, el cese de la respiración debido a una obstrucción total de las vías aéreas superiores. A veces el motivo de la preocupación de los familiares es comprobar que las apneas son cada vez más prolongadas, llegando hasta 60-90 seg, y producen cianosis. En ocasiones el final de una apnea se asocia a fuertes ronquidos, inspiraciones bruscas, gemidos o murmullos, o movimientos de todo el cuerpo.
Se caracteriza por interrupciones episódicas de la ventilación durante el sueño (apneas o hipoapneas) en ausencia de obstrucción de las vías aéreas. Por tanto, y a diferencia de las apneas obstructivas, las apneas centrales no se asocian a movimientos continuados de la pared torácica o abdominal y son más frecuentes en las personas de mayor edad como resultado de enfermedades cardíacas o neurológicas que afectan la regulación de la ventilación.
El motivo de consulta principal suele estar presidido por insomnio debido a frecuentes despertares, que el individuo puede o no asociar a dificultad respiratoria. Estos individuos también pueden ser roncadores de carácter leve, aunque no suelen acudir a la consulta por este hecho, dada su poca relevancia.
Se caracteriza por un deterioro del control de la ventilación que determina niveles arteriales de oxígeno anormalmente bajos, agravados sobre todo durante el sueño (hipoventilación sin apneas o hipoapneas). Los individuos con este trastorno conservan intactas las propiedades mecánicas de los pulmones. Esta forma de trastorno del sueño relacionado con la respiración incide casi siempre en individuos con sobrepeso y puede asociarse tanto a somnolencia excesiva como a insomnio.
Todos los trastornos del sueño relacionados con la respiración producen alteraciones específicas. Así, en el síndrome de apnea obstructiva del sueño los registros polisomnográficos nocturnos muestran episodios apneicos de más de 10 seg. de duración (habitualmente 20-40 seg.), siendo más raras las apneas que se prolongan más allá de varios minutos. Las hipoapneas se caracterizan por una reducción del flujo aéreo. Tanto las apneas como las hipoapneas se asocian a una reducción de la saturación de oxihemoglobina. En el síndrome de apnea obstructiva del sueño puede existir una respiración de Cheyne-Stokes al ser un patrón continuo que consiste en ciclos de una apnea, un episodio de hiperventilación de 10 a 60 seg. de duración y una disminución gradual de la ventilación que culmina en una nueva apnea (Tozzola, 2001).
Apneas, hipoapneas e hipoventilación pueden originar otras alteraciones: desaturación de la oxihemoglobina, alteraciones del EEG, incrementos de la tensión arterial pulmonar y sistémica, y aumentos transitorios de la activación a medida que el episodio de dificultad respiratoria se acerca a su fin. Los individuos con trastorno del sueño relacionado con la respiración suelen presentar arritmias durante el sueño, entre las cuales se incluyen arritmias sinusales, síndromes de preexcitación ventricular, bloqueos auriculoventriculares o paradas sinusales. Durante los episodios apneicos son frecuentes las bradicardias seguidas de taquicardia. La elevada frecuencia de los despertares nocturnos y la desaturación de la oxihemoglobina pueden dar lugar a somnolencia excesiva, la cual es detectable mediante un MSLT u otros tests para medir la somnolencia diurna. El MSLT suele poner de manifiesto una latencia media del sueño inferior a los 10 minutos, situándose incluso por debajo de los 5 minutos (cuando lo normal es 10-20) (Tozzola, 2001).
Las gasometrías arteriales cuando el individuo está despierto suelen proporcionar valores normales, pero en algunos casos graves de síndrome de apnea obstructiva del sueño o de síndrome de hipoventilación alveolar central se detecta hipoxemia o hipercapnia en la vigilia. Las radiografías cefalométricas, la resonancia magnética (RM), la tomografía computarizada (TC) y la práctica de endoscopias con cámaras de fibra óptica pueden poner de manifiesto una obstrucción de las vías aéreas superiores. Las pruebas cardíacas pueden mostrar un deterioro de la función ventricular derecha. En estos individuos cabe detectar también cifras elevadas de hemoglobina o del hematócrito motivadas por la hipoxemia nocturna sostenida (Tozzola, 2001).
El trastorno del sueño relacionado con la respiración puede asociarse a enfermedades neurológicas o médicas. Por ejemplo, la apnea obstructiva del sueño puede obedecer a un engrosamiento lingual secundario a: acromegalia, quistes tiroideos linguales de carácter ectópico o parálisis de las cuerdas vocales como la que se observa en el síndrome de Shy-Drager.
La característica esencial del trastorno del ritmo circadiano es la presencia persistente o recurrente de un patrón de sueño desestructurado que obedece a una mala sincronización entre el sistema circadiano endógeno de sueño-vigilia del individuo, por una parte, y las exigencias exógenas de espaciamiento y duración del sueño, por otra. A diferencia de otros trastornos del sueño primarios, el trastorno del ritmo circadiano no responde a los mecanismos generadores de sueño y vigilia per se. Debido a esta desincronización circadiana, los individuos con trastorno pueden aquejar insomnio en ciertos momentos del día y somnolencia excesiva en otros, lo que da lugar a un malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo. Los problemas de sueño no se explican mejor por la presencia de otros trastornos del sueño u otros trastornos mentales y no se deben a los efectos fisiológicos directos de una sustancia o una enfermedad médica. La capacidad de estos individuos para adaptarse a los cambios y requerimientos circadianos muestra amplias variaciones. Muchos, por no decir la mayoría, de los individuos con alteraciones del sueño relacionadas con el ritmo circadiano no solicitan ayuda terapéutica y no tienen síntomas lo bastante intensos como para permitir efectuar el diagnóstico. Los que acuden a la consulta con este trastorno suelen hacerlo porque el cuadro sintomático ha adquirido una intensidad o una persistencia insoportables. Por ejemplo, no es raro que los trabajadores que han cambiado de turno de trabajo acudan a la consulta después de haberse quedado dormidos durante el trabajo o mientras conducían.
El diagnóstico de trastorno del ritmo circadiano se basa principalmente en la historia clínica, que incluye el horario de trabajo, de sueño, de siestas y de «tiempo libre». La historia debe también reflejar los esfuerzos que estos individuos han realizado para enfrentarse a tales síntomas, por ejemplo, el intento de avanzar el ritmo de sueño-vigilia en el tipo de sueño retrasado. Los diarios de ritmo de sueño-vigilia o las tarjetas de registro prospectivas del sueño son a menudo valiosas armas diagnósticas.
Este tipo de trastorno del ritmo circadiano responde a un ciclo sueño-vigilia endógeno retrasado en relación con las demandas de la sociedad. La medición de los ritmos circadianos endógenos (como el de la temperatura corporal central) refleja claramente este retraso. Se han propuesto hipótesis de que los individuos que presentan este subtipo, muestran una capacidad anormalmente reducida para adelantar las fases de sueño-vigilia como es el avanzar el horario de acostarse y de levantarse. Como resultado de todo esto, estas personas están bloqueadas por un horario de sueño tardío y no pueden avanzarlo a horas más tempranas. La fase circadiana de sueño se comporta de forma estable: estos individuos, si se les permite en los fines de semana o en las vacaciones, se dormirán y despertarán con arreglo a unos horarios coherentes, aunque retrasados. Las personas afectas aquejan dificultad para dormir en las horas que aconseja la sociedad, pero, una vez que han conciliado el sueño, éste es completamente normal. Existe una dificultad concomitante para levantarse a las horas socialmente aceptadas. Puesto que muchos de estos individuos presentarán una deprivación crónica del sueño, puede aparecer somnolencia en momentos en que el individuo desearía estar despierto.
Los trabajadores que se someten a cambios de turno pueden mostrar una apariencia cansada o soñolienta y una mayor incidencia de trastornos cardiovasculares y gastrointestinales, por ejemplo, gastritis y enfermedad ulcerosa péptica. El papel del consumo de alcohol y cafeína y de la alteración de los patrones alimentarios en estos individuos todavía no ha sido estudiado en profundidad. La ausencia de patrón sueño-vigilia de 24 horas ocurre a menudo en las personas ciegas. El trastorno del ritmo circadiano puede exacerbar enfermedades médicas preexistentes.
En este tipo de trastorno del ritmo circadiano endógeno de sueño-vigilia es normal, y la alteración nace del conflicto entre este patrón endógeno de sueño-vigilia y el vigente en una zona con distinto huso horario. Estos individuos aquejan una desincronización entre el horario de sueño que ellos desean y el que les viene impuesto por la zona donde se encuentran.
La intensidad de esta descoordinación es proporcional al número de horas de diferencia existentes entre el lugar donde se encuentran y el lugar del que provienen, apareciendo a menudo las máximas dificultades cuando se supera la diferencia de 8 horas en menos de 1 día. Los viajes en sentido este, que conllevan un adelantamiento de las horas de sueño y de vigilia suelen representar un problema mayor que los viajes hacia el oeste, ritmo de sueño-vigilia retrasado.
Los síntomas del jet lag y de los cambios de turno de trabajo suelen describirse como más intensos, o más fácilmente inducibles, en las personas de edad mediana tardía o en los ancianos. El patrón de sueño avanzado también aumenta su frecuencia con la edad. Estos hechos pueden obedecer al deterioro del sueño nocturno y al acortamiento del período circadiano endógeno relacionados con la edad.
Los estudios experimentales y prácticos concernientes al jet lag indican que el sistema circadiano necesita 1 día por hora de diferencia para resincronizarse al nuevo huso horario. Otros ritmos circadianos como, por ejemplo, la temperatura corporal central, el nivel hormonal, el estado de alerta y los patrones de sueño, requieren más o menos tiempo para reajustarse también.
En este tipo de trastorno del ritmo circadiano el ciclo circadiano endógeno de sueño-vigilia es normal, y la alteración nace del conflicto entre este patrón de sueño-vigilia generado por el sistema circadiano y el nuevo patrón que exige un cambio de turno de trabajo. Los trabajadores sometidos a frecuentes rotaciones en el turno de trabajo son los que tienen más dificultades, ya que fuerzan el sueño y la vigilia en función de un ritmo circadiano aberrante, lo que imposibilita cualquier intento de adaptación. Los trabajadores de noche o los que se ven sometidos a frecuentes rotaciones en el turno de trabajo muestran típicamente una menor duración del sueño y una mayor frecuencia de alteraciones en la continuidad del sueño en comparación con los trabajadores de mañana y tarde. En cambio, también pueden presentar un mayor grado de somnolencia durante el período en que desearían estar despiertos, es decir, en mitad de la noche, tal como exige su turno de trabajo. La desincronización circadiana de este tipo suele exacerbarse a causa de unas horas de sueño insuficiente, exigencias sociales y familiares y alteraciones ambientales que perturban sus momentos de descanso.
Este tipo de trastorno del ritmo circadiano debe indicarse si hay otra alteración del patrón de sueño circadiano, como es el patrón de sueño avanzado, ausencia de patrón sueño-vigilia de 24 horas o patrón de sueño-vigilia irregular. El «patrón de sueño avanzado» es el análogo del tipo sueño retrasado, pero en sentido opuesto: los individuos aquejan incapacidad para mantenerse despiertos en las últimas horas de la tarde y despertares espontáneos en plena madrugada. La «ausencia de patrón sueño-vigilia de 24 horas» denota la presencia de horarios libres: el ritmo de sueño-vigilia sigue un ciclo circadiano de aproximadamente 24-25 horas, mientras que los acontecimientos y estímulos ambientales conforman períodos definidos de 24 horas. A diferencia del patrón sueño-vigilia estable, característico de los tipos sueño retrasado o avanzado, el ritmo sueño-vigilia de estos individuos se retrasa cada vez más respecto al lapso de 24 horas, dando lugar, con el paso de los días, a patrones de sueño-vigilia cambiantes. El «patrón de sueño-vigilia irregular» indica la ausencia de un patrón sueño-vigilia identificable.
La ausencia de patrón sueño-vigilia de 24 horas se ha asociado con rasgos de personalidad de tipo esquizoide. Los tipos jet lag y cambios de turno de trabajo pueden provocar o exacerbar un episodio maníaco o depresivo mayor o un brote de un trastorno psicótico.
Esta categoría se reserva para los cuadros clínicos de insomnio, hipersomnia o alteraciones del ritmo circadiano que no reúnen criterios para una disomnia específica. Son ejemplos:
1. Quejas de insomnio o hipersomnia clínicamente significativos que pueden atribuirse a factores ambientales como son el ruido, luz, interrupciones frecuentes, etc.
2. Somnolencia excesiva atribuible a una deprivación concomitante de sueño.
3. "Síndrome de piernas inquietas" idiopático: sensación molesta (malestar, hormigueo o inquietud) que produce una intensa necesidad de mover las piernas. Típicamente estas sensaciones aparecen antes de acostarse y se alivian temporalmente moviendo las piernas o andando, volviendo a aparecer sólo si éstas se mantienen inmóviles. Estas sensaciones pueden retrasar el inicio del sueño o despertar al individuo.
4. "Movimientos periódicos de los miembros" (mioclonus nocturno): sacudidas de los miembros repetidas, breves y de baja amplitud, sobre todo de las extremidades inferiores. Estos movimientos aparecen cuando el individuo está a punto de dormirse y disminuyen durante las fases 3 y 4 NREM. Estos movimientos suelen aparecer rítmicamente cada 20-60 segundos, dando lugar a activaciones breves y repetidas. Característicamente, estos individuos no son conscientes de estos movimientos, pero sí pueden aquejar insomnio, despertares frecuentes o somnolencia diurna si el número de movimientos es considerable.
5. Situaciones en las que el clínico ha establecido la presencia de un trastorno del sueño, pero se ve incapaz de determinar si éste es primario, secundario a una enfermedad médica o relacionado con el consumo de una sustancia.
Insomnio primario
La característica esencial del insomnio primario es la dificultad para iniciar o mantener el sueño, o la sensación de no haber tenido un sueño reparador durante al menos 1 mes, que provoca un malestar clínicamente significativo o un deterioro laboral, social o de otras áreas importantes de la actividad del individuo. Esta alteración no aparece exclusivamente en el transcurso de otro trastorno del sueño u otro trastorno mental y no es debida a los efectos fisiológicos directos de una sustancia o de una enfermedad médica :
Evaluación del insomnio crónico (Adaptado de Reynolds, Buysse y Kuofer, 1996)
|
Paso 1 Evaluar la presencia de una patología orgánica que pueda afectar de forma negativa al sueño. Paso 2 Evaluar si algún fármaco o sustancia está alterando el sueño. Paso 3 Evaluar si otro trastorno mental como la depresión, esquizofrenia, trastorno por ansiedad, etc. está produciendo una alteración del sueño. Paso 4 Considerar una alteración respiratoria que produzca trastornos en el sueño si el paciente ronca o está obeso. Paso 5 Considerar un trastorno del ritmo sueño-vigilia si el paciente presenta un ritmo irregular o trabaja por turnos. Paso 6 Considerar el diagnóstico de una parasomnia si el paciente presenta molestias de sucesos conductuales o mentales que se producen durante el sueño. Paso 7 Si el insomnio dura más de un mes y no está relacionado con los anteriores trastornos, el diagnóstico es de insomnio primario. Paso 8 Si el cuadro de insomnio no se describe a partir de los criterios anteriores, se diagnosticará una disomnia anteriormente no especificada. |
Los individuos con insomnio primario presentan muy a menudo una combinación de dificultades para dormir y despertares frecuentes durante la noche. Con menos frecuencia se quejan únicamente de no tener un sueño reparador, es decir, tienen la sensación de que su sueño ha sido inquieto, poco profundo y de poca calidad. Este trastorno se suele asociar con un aumento del nivel de alerta fisiológica y psicológica durante la noche, junto a un condicionamiento negativo para dormir.
La preocupación intensa y el malestar por la imposibilidad de dormir bien pueden generar un círculo vicioso: cuanto más intenta el individuo dormir, más frustrado y molesto se encuentra, y menos duerme. Estar acostado en una cama en la que la persona ha pasado a menudo noches sin dormir puede producir frustración y activación condicionada. Por el contrario, el individuo puede dormirse más fácilmente cuando no lo intenta (mientras mira la televisión, lee o conduce el coche). Algunas personas con un estado de alerta alto y un acondicionamiento negativo explican que duermen mejor fuera de su dormitorio y de su entorno. El insomnio crónico puede provocar una disminución de la sensación de bienestar durante el día (alteración del estado de ánimo y de la motivación; atención, energía y concentración disminuidas, y un aumento de la sensación de fatiga y malestar).
Hipersomnia primaria
La característica esencial de la hipersomnia primaria es una somnolencia excesiva durante al menos 1 mes, evidenciada tanto por episodios prolongados de sueño como por episodios de sueño diurno que se producen prácticamente cada día. La somnolencia excesiva debe ser de suficiente gravedad como para provocar malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo; no aparece exclusivamente en el transcurso de otro trastorno del sueño o de otro trastorno mental, ni se debe a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
En los individuos con hipersomnia primaria la duración del episodio de sueño más largo (para la mayoría de las personas, el sueño nocturno) oscila entre 8 y 12 horas, y a menudo se acompaña de problemas a la hora de levantarse. La calidad real del sueño nocturno es normal. La somnolencia excesiva durante las horas habituales de vigilia toma la forma de siestas intencionadas o de episodios de sueño inadvertidos. Las determinaciones objetivas demuestran una somnolencia fisiológica aumentada. Las siestas durante el día tienden a ser relativamente largas, el individuo no nota que sean reparadoras y no producen una mejora en el nivel de alerta. Habitualmente, las personas que padecen este trastorno presentan la somnolencia de forma creciente a lo largo de un período de tiempo determinado, no experimentando «ataques» repentinos de sueño. Los episodios de sueño no intencionados tienen lugar habitualmente en situaciones de baja estimulación y baja actividad como durante conferencias, leyendo, mirando la televisión o conduciendo.
La hipersomnia puede provocar malestar significativo y deterioro social y laboral. El sueño nocturno prolongado y la dificultad para levantarse pueden producir problemas a la hora de cumplir con las obligaciones laborales. Los episodios no intencionados de sueño durante el día son a veces muy molestos e incluso peligrosos si, por ejemplo, el individuo está conduciendo o trabajando con una máquina. El nivel de alerta disminuido que se observa cuando el sujeto intenta combatir la somnolencia puede comportar un bajo rendimiento, una pobre concentración y un déficit de memoria durante las actividades diurnas.
La mayoría de los individuos con hipersomnia primaria tienen síntomas persistentes y de importancia. En la forma recidivante de la hipersomnia primaria, conocida como síndrome de Kleine-Levin, los individuos pueden llegar a pasar 18-20 horas durmiendo o en la cama. Los episodios recidivantes de somnolencia se asocian a otras características clínicas de desinhibición: hipersexualidad indiscriminada, episodios de ingesta excesiva y compulsiva, con ganancia de peso y en algunos individuos se han descrito irritabilidad, despersonalización, depresión, confusión y alucinaciones ocasionales, así como comportamientos impulsivos.
Narcolepsia
La característica esencial de la narcolepsia es la aparición recurrente e irresistible de sueño reparador, cataplejía e intrusiones recurrentes de elementos característicos de la fase REM en el período de transición entre el sueño y la vigilia. La somnolencia del individuo disminuye típicamente tras el ataque de sueño y sólo reaparece varias horas después. Los ataques de sueño han de ocurrir diariamente en un período de al menos 3 meses para poder establecer el diagnóstico aunque la mayoría de los individuos manifiesta haber padecido ataques de sueño durante muchos años antes de solicitar ayuda terapéutica. Además de somnolencia, los individuos con narcolepsia experimentan uno o ambos de los siguientes síntomas: cataplejía (es decir, episodios súbitos de pérdida bilateral del tono muscular que duran entre segundos y minutos y que suelen estar desencadenados por emociones intensas) o intrusiones recurrentes de elementos característicos de la fase REM en el período de transición que va del sueño a la vigilia y que se traducen en parálisis de los músculos voluntarios o alucinaciones de carácter onírico. Los síntomas no se deben a los efectos fisiológicos directos de una sustancia (incluyendo fármacos) o de otra enfermedad médica. Los episodios de somnolencia de la narcolepsia suelen describirse como irresistibles, dando lugar a sueño de carácter involuntario en situaciones claramente inadecuadas como puede ser al mantener una conversación. Las situaciones poco estimulantes o poco activas exacerban típicamente el grado de somnolencia.
Los episodios de sueño suelen durar 10 a 20 minutos, pudiendo llegar a horas si no se ven interrumpidos. Es frecuente que estos individuos relaten actividad onírica durante tales episodios. Las personas que padecen narcolepsia disponen de diversas estrategias para «neutralizar» estos ataques de sueño. Cuando no se sigue tratamiento, el número de episodios diarios de sueño (intencionado o no intencionado) se sitúa entre 2 y 6. Los episodios de sueño suelen aparecer sobre un nivel de alerta relativamente normal, aunque algunos individuos confiesan presentar de forma constante algún grado de somnolencia. La cataplejía acostumbra a aparecer varios años después de establecida la somnolencia diurna e incide aproximadamente en un 70 % de los individuos que sufren el trastorno. En la cataplejía la pérdida del tono muscular debe ser de carácter brusco, dando lugar a una caída de la mandíbula, la cabeza o los brazos, no observable por los demás. A veces la cataplejía reviste un carácter mucho más espectacular, y así, al individuo pueden caérsele objetos que esté transportando, puede desplomarse sobre sus rodillas o caerse realmente al suelo. La musculatura respiratoria y ocular está respetada. La debilidad muscular suele durar sólo unos segundos, aunque se han descrito episodios de hasta media hora de duración. La recuperación de la fuerza muscular es total e inmediata. Durante los episodios estos individuos conservan la conciencia y el estado de alerta, de forma que son capaces de describir perfectamente y sin confusión todo lo que ha ocurrido en ese momento. Aunque no es frecuente, los ataques prolongados de cataplejía pueden desembocar en episodios de sueño. La cataplejía suele estar desencadenada por estímulos emocionales intensos. La deprivación del sueño aumenta la frecuencia y la intensidad de los episodios de cataplejía. Aproximadamente el 20-40 % de los individuos con narcolepsia presenta asimismo imágenes que recuerdan mucho los sueños justo antes de quedarse dormidos (alucinaciones hipnagógicas) o justo después de despertarse (alucinaciones hipnopómpicas). La mayor parte de las alucinaciones relacionadas con el sueño son de carácter visual e incorporan elementos del entorno real. Las alucinaciones también son de carácter auditivo o cinético. Aproximadamente el 30-50 % de los individuos con narcolepsia experimenta asimismo parálisis del sueño justo en el preciso momento de dormirse o despertarse. En este trastorno los individuos describen estar despiertos, pero son incapaces de moverse o hablar. También pueden aquejar incapacidad para respirar; lo cierto es que el diafragma deja de trabajar, si bien la respiración no se detiene. Las alucinaciones relacionadas con el sueño y las parálisis del sueño aparecen a veces de forma simultánea, lo que lugar a una experiencia terrorífica de ver y/o escuchar cosas inusuales sin poder escapar, pudiendo durar entre segundos a minutos.
En aproximadamente un 40 % de los individuos con narcolepsia se detecta un trastorno mental actual o pasado. Entre los trastornos asociados más a menudo se encuentran los trastornos del estado de ánimo (especialmente el trastorno depresivo mayor y la distimia), seguidos de los trastornos relacionados con sustancias y el trastorno de ansiedad generalizada. También presentan una mayor incidencia de antecedentes de parasomnias como sonambulismo, bruxismo (cierre de la mandíbula y rechinar de los dientes), y enuresis.
Trastorno del sueño relacionado con la respiración
La característica esencial de este trastorno es una desestructuración del sueño que da lugar a somnolencia excesiva o insomnio, y que se considera secundaria a alteraciones de la ventilación durante el sueño (p. ej. , apnea del sueño o hipoventilación alveolar central). La somnolencia excesiva constituye el motivo de consulta más frecuente de los individuos con trastorno del sueño relacionado con la respiración. Esta somnolencia está producida por los frecuentes aumentos de activación que lleva a cabo el individuo durante el sueño nocturno en un intento por respirar de forma normal. La somnolencia se hace más patente en situaciones de relajación como leer o ver la televisión. La incapacidad del individuo para controlar esta somnolencia puede hacerse evidente revistiendo un carácter extremo, y la persona puede quedarse dormida incluso en situaciones activas como hablar, comer, andar o conducir.
Algunos individuos aquejan dificultad para respirar en posición supina o al dormir. Entre las alteraciones respiratorias que tienen lugar durante el sueño en este trastorno se incluyen las apneas que son episodios de interrupción de la respiración, hipoapneas (respiración anormalmente lenta o superficial) e hipoventilación (niveles sanguíneos de oxígeno y dióxido de carbono anormales). Se han descrito tres formas de trastorno del sueño relacionado con la respiración:
Síndrome de apnea obstructiva del sueño
Es la forma más frecuente de trastorno del sueño relacionado con la respiración. Se caracteriza por episodios repetidos de obstrucción de las vías aéreas superiores (apneas o hipoapneas) durante el sueño. Los impulsos nerviosos que rigen los movimientos respiratorios en el tórax y el abdomen están preservados. Esta forma del trastorno del sueño relacionado con la respiración suele incidir en individuos con sobrepeso y conducir a un estado de somnolencia excesiva. El síndrome de apnea obstructiva del sueño se caracteriza por ronquidos intensos o inspiraciones bruscas breves que alternan con episodios de silencio respiratorio que suelen durar 20-30 seg. Los ronquidos obedecen al paso de aire por unas vías aéreas parcialmente obstruidas. Los períodos de silencio respiratorio traducen las propias apneas obstructivas, es decir, el cese de la respiración debido a una obstrucción total de las vías aéreas superiores. A veces el motivo de la preocupación de los familiares es comprobar que las apneas son cada vez más prolongadas, llegando hasta 60-90 seg, y producen cianosis. En ocasiones el final de una apnea se asocia a fuertes ronquidos, inspiraciones bruscas, gemidos o murmullos, o movimientos de todo el cuerpo.
Síndrome de apnea central del sueño
Se caracteriza por interrupciones episódicas de la ventilación durante el sueño (apneas o hipoapneas) en ausencia de obstrucción de las vías aéreas. Por tanto, y a diferencia de las apneas obstructivas, las apneas centrales no se asocian a movimientos continuados de la pared torácica o abdominal y son más frecuentes en las personas de mayor edad como resultado de enfermedades cardíacas o neurológicas que afectan la regulación de la ventilación.
El motivo de consulta principal suele estar presidido por insomnio debido a frecuentes despertares, que el individuo puede o no asociar a dificultad respiratoria. Estos individuos también pueden ser roncadores de carácter leve, aunque no suelen acudir a la consulta por este hecho, dada su poca relevancia.
Síndrome de hipoventilación alveolar central
Se caracteriza por un deterioro del control de la ventilación que determina niveles arteriales de oxígeno anormalmente bajos, agravados sobre todo durante el sueño (hipoventilación sin apneas o hipoapneas). Los individuos con este trastorno conservan intactas las propiedades mecánicas de los pulmones. Esta forma de trastorno del sueño relacionado con la respiración incide casi siempre en individuos con sobrepeso y puede asociarse tanto a somnolencia excesiva como a insomnio.
Todos los trastornos del sueño relacionados con la respiración producen alteraciones específicas. Así, en el síndrome de apnea obstructiva del sueño los registros polisomnográficos nocturnos muestran episodios apneicos de más de 10 seg. de duración (habitualmente 20-40 seg.), siendo más raras las apneas que se prolongan más allá de varios minutos. Las hipoapneas se caracterizan por una reducción del flujo aéreo. Tanto las apneas como las hipoapneas se asocian a una reducción de la saturación de oxihemoglobina. En el síndrome de apnea obstructiva del sueño puede existir una respiración de Cheyne-Stokes al ser un patrón continuo que consiste en ciclos de una apnea, un episodio de hiperventilación de 10 a 60 seg. de duración y una disminución gradual de la ventilación que culmina en una nueva apnea (Tozzola, 2001).
Apneas, hipoapneas e hipoventilación pueden originar otras alteraciones: desaturación de la oxihemoglobina, alteraciones del EEG, incrementos de la tensión arterial pulmonar y sistémica, y aumentos transitorios de la activación a medida que el episodio de dificultad respiratoria se acerca a su fin. Los individuos con trastorno del sueño relacionado con la respiración suelen presentar arritmias durante el sueño, entre las cuales se incluyen arritmias sinusales, síndromes de preexcitación ventricular, bloqueos auriculoventriculares o paradas sinusales. Durante los episodios apneicos son frecuentes las bradicardias seguidas de taquicardia. La elevada frecuencia de los despertares nocturnos y la desaturación de la oxihemoglobina pueden dar lugar a somnolencia excesiva, la cual es detectable mediante un MSLT u otros tests para medir la somnolencia diurna. El MSLT suele poner de manifiesto una latencia media del sueño inferior a los 10 minutos, situándose incluso por debajo de los 5 minutos (cuando lo normal es 10-20) (Tozzola, 2001).
Las gasometrías arteriales cuando el individuo está despierto suelen proporcionar valores normales, pero en algunos casos graves de síndrome de apnea obstructiva del sueño o de síndrome de hipoventilación alveolar central se detecta hipoxemia o hipercapnia en la vigilia. Las radiografías cefalométricas, la resonancia magnética (RM), la tomografía computarizada (TC) y la práctica de endoscopias con cámaras de fibra óptica pueden poner de manifiesto una obstrucción de las vías aéreas superiores. Las pruebas cardíacas pueden mostrar un deterioro de la función ventricular derecha. En estos individuos cabe detectar también cifras elevadas de hemoglobina o del hematócrito motivadas por la hipoxemia nocturna sostenida (Tozzola, 2001).
El trastorno del sueño relacionado con la respiración puede asociarse a enfermedades neurológicas o médicas. Por ejemplo, la apnea obstructiva del sueño puede obedecer a un engrosamiento lingual secundario a: acromegalia, quistes tiroideos linguales de carácter ectópico o parálisis de las cuerdas vocales como la que se observa en el síndrome de Shy-Drager.
Trastorno del ritmo circadiano
La característica esencial del trastorno del ritmo circadiano es la presencia persistente o recurrente de un patrón de sueño desestructurado que obedece a una mala sincronización entre el sistema circadiano endógeno de sueño-vigilia del individuo, por una parte, y las exigencias exógenas de espaciamiento y duración del sueño, por otra. A diferencia de otros trastornos del sueño primarios, el trastorno del ritmo circadiano no responde a los mecanismos generadores de sueño y vigilia per se. Debido a esta desincronización circadiana, los individuos con trastorno pueden aquejar insomnio en ciertos momentos del día y somnolencia excesiva en otros, lo que da lugar a un malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo. Los problemas de sueño no se explican mejor por la presencia de otros trastornos del sueño u otros trastornos mentales y no se deben a los efectos fisiológicos directos de una sustancia o una enfermedad médica. La capacidad de estos individuos para adaptarse a los cambios y requerimientos circadianos muestra amplias variaciones. Muchos, por no decir la mayoría, de los individuos con alteraciones del sueño relacionadas con el ritmo circadiano no solicitan ayuda terapéutica y no tienen síntomas lo bastante intensos como para permitir efectuar el diagnóstico. Los que acuden a la consulta con este trastorno suelen hacerlo porque el cuadro sintomático ha adquirido una intensidad o una persistencia insoportables. Por ejemplo, no es raro que los trabajadores que han cambiado de turno de trabajo acudan a la consulta después de haberse quedado dormidos durante el trabajo o mientras conducían.
El diagnóstico de trastorno del ritmo circadiano se basa principalmente en la historia clínica, que incluye el horario de trabajo, de sueño, de siestas y de «tiempo libre». La historia debe también reflejar los esfuerzos que estos individuos han realizado para enfrentarse a tales síntomas, por ejemplo, el intento de avanzar el ritmo de sueño-vigilia en el tipo de sueño retrasado. Los diarios de ritmo de sueño-vigilia o las tarjetas de registro prospectivas del sueño son a menudo valiosas armas diagnósticas.
Dentro de los trastornos del ritmo circadiano, diferenciamos:
Tipo de sueño retrasado
Este tipo de trastorno del ritmo circadiano responde a un ciclo sueño-vigilia endógeno retrasado en relación con las demandas de la sociedad. La medición de los ritmos circadianos endógenos (como el de la temperatura corporal central) refleja claramente este retraso. Se han propuesto hipótesis de que los individuos que presentan este subtipo, muestran una capacidad anormalmente reducida para adelantar las fases de sueño-vigilia como es el avanzar el horario de acostarse y de levantarse. Como resultado de todo esto, estas personas están bloqueadas por un horario de sueño tardío y no pueden avanzarlo a horas más tempranas. La fase circadiana de sueño se comporta de forma estable: estos individuos, si se les permite en los fines de semana o en las vacaciones, se dormirán y despertarán con arreglo a unos horarios coherentes, aunque retrasados. Las personas afectas aquejan dificultad para dormir en las horas que aconseja la sociedad, pero, una vez que han conciliado el sueño, éste es completamente normal. Existe una dificultad concomitante para levantarse a las horas socialmente aceptadas. Puesto que muchos de estos individuos presentarán una deprivación crónica del sueño, puede aparecer somnolencia en momentos en que el individuo desearía estar despierto.
Los trabajadores que se someten a cambios de turno pueden mostrar una apariencia cansada o soñolienta y una mayor incidencia de trastornos cardiovasculares y gastrointestinales, por ejemplo, gastritis y enfermedad ulcerosa péptica. El papel del consumo de alcohol y cafeína y de la alteración de los patrones alimentarios en estos individuos todavía no ha sido estudiado en profundidad. La ausencia de patrón sueño-vigilia de 24 horas ocurre a menudo en las personas ciegas. El trastorno del ritmo circadiano puede exacerbar enfermedades médicas preexistentes.
Tipo jet lag
En este tipo de trastorno del ritmo circadiano endógeno de sueño-vigilia es normal, y la alteración nace del conflicto entre este patrón endógeno de sueño-vigilia y el vigente en una zona con distinto huso horario. Estos individuos aquejan una desincronización entre el horario de sueño que ellos desean y el que les viene impuesto por la zona donde se encuentran.
La intensidad de esta descoordinación es proporcional al número de horas de diferencia existentes entre el lugar donde se encuentran y el lugar del que provienen, apareciendo a menudo las máximas dificultades cuando se supera la diferencia de 8 horas en menos de 1 día. Los viajes en sentido este, que conllevan un adelantamiento de las horas de sueño y de vigilia suelen representar un problema mayor que los viajes hacia el oeste, ritmo de sueño-vigilia retrasado.
Los síntomas del jet lag y de los cambios de turno de trabajo suelen describirse como más intensos, o más fácilmente inducibles, en las personas de edad mediana tardía o en los ancianos. El patrón de sueño avanzado también aumenta su frecuencia con la edad. Estos hechos pueden obedecer al deterioro del sueño nocturno y al acortamiento del período circadiano endógeno relacionados con la edad.
Los estudios experimentales y prácticos concernientes al jet lag indican que el sistema circadiano necesita 1 día por hora de diferencia para resincronizarse al nuevo huso horario. Otros ritmos circadianos como, por ejemplo, la temperatura corporal central, el nivel hormonal, el estado de alerta y los patrones de sueño, requieren más o menos tiempo para reajustarse también.
Tipo cambios de turno de trabajo
En este tipo de trastorno del ritmo circadiano el ciclo circadiano endógeno de sueño-vigilia es normal, y la alteración nace del conflicto entre este patrón de sueño-vigilia generado por el sistema circadiano y el nuevo patrón que exige un cambio de turno de trabajo. Los trabajadores sometidos a frecuentes rotaciones en el turno de trabajo son los que tienen más dificultades, ya que fuerzan el sueño y la vigilia en función de un ritmo circadiano aberrante, lo que imposibilita cualquier intento de adaptación. Los trabajadores de noche o los que se ven sometidos a frecuentes rotaciones en el turno de trabajo muestran típicamente una menor duración del sueño y una mayor frecuencia de alteraciones en la continuidad del sueño en comparación con los trabajadores de mañana y tarde. En cambio, también pueden presentar un mayor grado de somnolencia durante el período en que desearían estar despiertos, es decir, en mitad de la noche, tal como exige su turno de trabajo. La desincronización circadiana de este tipo suele exacerbarse a causa de unas horas de sueño insuficiente, exigencias sociales y familiares y alteraciones ambientales que perturban sus momentos de descanso.
Tipo no especificado
Este tipo de trastorno del ritmo circadiano debe indicarse si hay otra alteración del patrón de sueño circadiano, como es el patrón de sueño avanzado, ausencia de patrón sueño-vigilia de 24 horas o patrón de sueño-vigilia irregular. El «patrón de sueño avanzado» es el análogo del tipo sueño retrasado, pero en sentido opuesto: los individuos aquejan incapacidad para mantenerse despiertos en las últimas horas de la tarde y despertares espontáneos en plena madrugada. La «ausencia de patrón sueño-vigilia de 24 horas» denota la presencia de horarios libres: el ritmo de sueño-vigilia sigue un ciclo circadiano de aproximadamente 24-25 horas, mientras que los acontecimientos y estímulos ambientales conforman períodos definidos de 24 horas. A diferencia del patrón sueño-vigilia estable, característico de los tipos sueño retrasado o avanzado, el ritmo sueño-vigilia de estos individuos se retrasa cada vez más respecto al lapso de 24 horas, dando lugar, con el paso de los días, a patrones de sueño-vigilia cambiantes. El «patrón de sueño-vigilia irregular» indica la ausencia de un patrón sueño-vigilia identificable.
La ausencia de patrón sueño-vigilia de 24 horas se ha asociado con rasgos de personalidad de tipo esquizoide. Los tipos jet lag y cambios de turno de trabajo pueden provocar o exacerbar un episodio maníaco o depresivo mayor o un brote de un trastorno psicótico.
Disomnia no especificada
Esta categoría se reserva para los cuadros clínicos de insomnio, hipersomnia o alteraciones del ritmo circadiano que no reúnen criterios para una disomnia específica. Son ejemplos:
1. Quejas de insomnio o hipersomnia clínicamente significativos que pueden atribuirse a factores ambientales como son el ruido, luz, interrupciones frecuentes, etc.
2. Somnolencia excesiva atribuible a una deprivación concomitante de sueño.
3. "Síndrome de piernas inquietas" idiopático: sensación molesta (malestar, hormigueo o inquietud) que produce una intensa necesidad de mover las piernas. Típicamente estas sensaciones aparecen antes de acostarse y se alivian temporalmente moviendo las piernas o andando, volviendo a aparecer sólo si éstas se mantienen inmóviles. Estas sensaciones pueden retrasar el inicio del sueño o despertar al individuo.
4. "Movimientos periódicos de los miembros" (mioclonus nocturno): sacudidas de los miembros repetidas, breves y de baja amplitud, sobre todo de las extremidades inferiores. Estos movimientos aparecen cuando el individuo está a punto de dormirse y disminuyen durante las fases 3 y 4 NREM. Estos movimientos suelen aparecer rítmicamente cada 20-60 segundos, dando lugar a activaciones breves y repetidas. Característicamente, estos individuos no son conscientes de estos movimientos, pero sí pueden aquejar insomnio, despertares frecuentes o somnolencia diurna si el número de movimientos es considerable.
5. Situaciones en las que el clínico ha establecido la presencia de un trastorno del sueño, pero se ve incapaz de determinar si éste es primario, secundario a una enfermedad médica o relacionado con el consumo de una sustancia.
Son trastornos caracterizados por comportamientos o fenómenos fisiológicos anormales que tienen lugar coincidiendo con el sueño, con algunas de sus fases específicas o con las transiciones sueño-vigilia. A diferencia de los trastornos del sueño, las parasomnias no implican una anormalidad de los mecanismos que rigen el ritmo circadiano ni de los horarios de sueño y despertar. En realidad, las parasomnias representan la activación de sistemas fisiológicos en momentos inapropiados del ciclo sueño-vigilia.
En concreto, estos trastornos conllevan la activación del sistema nervioso vegetativo, del sistema motor o de los procesos cognoscitivos durante el sueño o las transiciones sueño-vigilia. Cada parasomnia afecta una fase característica del sueño, de forma que a menudo cada tipo específico de parasomnia incide en una fase de sueño concreta. Las personas con parasomnias suelen acudir a la consulta debido a comportamientos extraños durante el sueño más que por quejas de insomnio o somnolencia diurna excesiva. Comprenden a estas Parasomnias: las pesadillas, los terrores nocturnos, el sonambulismo y la parasomnia no especificada.
La característica esencial de este trastorno es la aparición repetida de sueños terroríficos que despiertan al individuo, pasando éste a un estado totalmente vigil. Los sueños terroríficos o la interrupción sistemática del descanso nocturno provocan un malestar clínicamente significativo o un deterioro social o laboral. Este diagnóstico no debe efectuarse si las pesadillas aparecen exclusivamente en el transcurso de otro trastorno mental o se deben a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
Las pesadillas toman la forma típica de un sueño largo y elaborado que provoca una intensa ansiedad o terror. El contenido de estos sueños suele centrarse en peligros físicos inminentes para el individuo. Las pesadillas que aparecen después de experiencias traumáticas pueden recrear esta situación original, si bien la mayoría de ellas no hacen referencia a acontecimientos reales. Al despertar, los individuos con este trastorno son capaces de describir la secuencia del sueño con detalle; a veces relatan haber tenido múltiples pesadillas en una misma noche, a menudo centradas en un tema recurrente.
Las pesadillas aparecen casi exclusivamente en el sueño REM, y, como estos episodios REM ocurren de forma periódica a lo largo del sueño nocturno, aproximadamente cada 90-110 min., las pesadillas pueden estar en cualquier momento de la noche. No obstante, como los períodos de sueño REM se hacen típicamente prolongados y el componente onírico adquiere más intensidad en la segunda mitad de la noche, las pesadillas también tienen más probabilidades de aparecer en esta segunda mitad.
Las pesadillas suelen terminar con el despertar del individuo, que se asocia a un rápido retorno al estado de plena alerta y a una sensación prolongada de miedo o ansiedad. Sin embargo, si los despertares nocturnos son frecuentes o el individuo evita dormir por miedo a las pesadillas, puede aparecer somnolencia excesiva, dificultades para la concentración, depresión, ansiedad o irritabilidad.
En estos individuos son frecuentes los síntomas de depresión o ansiedad que no reúnen los criterios diagnósticos de un trastorno específico. Debido a la pérdida de tono muscular característica del sueño REM, es raro que aparezcan movimientos corporales o vocalizaciones.
Las palabras, gritos o sacudidas suelen ser un fenómeno de breve duración que anuncia el final de la pesadilla y son más característicos de las pesadillas que acompañan al trastorno por estrés postraumático, ya que éstas tienen lugar en el sueño NREM.
La característica esencial de este trastorno es la aparición repetida de terrores nocturnos, es decir, despertares bruscos que suelen estar precedidos por gritos o lloros de angustia.
Los terrores nocturnos suelen hacer acto de presencia durante el primer tercio del sueño y prolongarse por espacio de 1-10 min. Estos episodios se acompañan de activación vegetativa y manifestaciones comportamentales de miedo intenso. Durante el episodio, es difícil despertar o calmar al individuo. De todas formas, si éste consigue despertarse, no recuerda nada del contenido del terror o bien sólo imágenes fragmentadas y aisladas. Al levantarse por la mañana, es típica la amnesia sobre lo acontecido durante la noche. Los episodios de terror nocturno provocan un malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo.
Es típico que durante uno de estos episodios el individuo se siente bruscamente en la cama y empiece a gritar o a llorar, mostrando una expresión facial de terror y signos vegetativos de intensa ansiedad como taquicardia, taquipnea, enrojecimiento, sudoración, dilatación pupilar, aumento del tono muscular. El individuo no suele responder a los esfuerzos de los demás por despertarlo o calmarlo. Si por fin logra despertarse, se muestra confuso y desorientado durante unos minutos y describe una vaga sensación de terror, a menudo sin componente onírico asociado.
Los individuos con trastorno por estrés postraumático y el trastorno de ansiedad generalizada, tienen asimismo un riesgo mayor de padecer terrores nocturnos. Los individuos con terrores nocturnos, por su parte, pueden presentar trastornos de la personalidad, en especial trastornos dependiente y límite de la personalidad. Los tests e inventarios de personalidad practicados en estos individuos arrojan altas puntuaciones para la depresión y la ansiedad.
La característica esencial del sonambulismo es la existencia de episodios repetidos de comportamientos motores complejos que se inician durante el sueño y que implican que el individuo se levante de la cama y empiece a andar. Los episodios de sonambulismo suceden durante las fases de sueño con actividad EEG lenta y, por tanto, suelen aparecer en el primer tercio de la noche. Durante estos episodios, el individuo presenta una disminución del estado vigil y de la reactividad a los estímulos, mirada fija y perdida, y una ausencia relativa de respuesta al diálogo o a los esfuerzos que emprenden los demás para despertarlo. Si logra despertarse durante uno de estos episodios, el individuo no consigue recordarlo con claridad. Después del episodio, puede aparecer un breve período de confusión en un primer momento, que suele seguirse de una recuperación total de las funciones cognoscitivas y del comportamiento normal. El sonambulismo debe provocar malestar clínicamente significativo. No debe establecerse el diagnóstico de sonambulismo si el comportamiento que lleva a cabo el individuo por la noche se debe a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
Los episodios de sonambulismo pueden terminar en forma de despertar espontáneo que se sigue de breves períodos de confusión; en otras ocasiones el individuo vuelve a acostarse y sigue durmiendo como si nada hubiera pasado. No es raro que a la mañana siguiente el individuo se despierte en otros lugares o encuentre pruebas de haber llevado a cabo algunas actividades durante la noche, aunque de todas formas la amnesia preside el recuerdo de estos acontecimientos. La articulación de la palabra es pobre, y es raro que se establezcan diálogos, pueden obedecer los requerimientos de otras personas para que cesen en su actividad y retornen a la cama. De todas formas, todos estos comportamientos están presididos por un bajo nivel de vigilancia, de modo que despertar al sujeto en pleno episodio resulta característicamente muy difícil. Si logra despertarse, permanece confuso durante unos minutos y posteriormente recupera el estado de vigilia normal.
Los individuos con sonambulismo pueden presentar asimismo otras parasomnias asociadas al sueño NREM como son los terrores nocturnos. En los niños el sonambulismo no suele coexistir con otros trastornos mentales, pero en los adultos esto sí puede suceder, sobre todo con trastornos de la personalidad, trastornos del estado de ánimo o trastornos de ansiedad.
El sonambulismo incide por igual en varones y mujeres. La máxima prevalencia se sitúa alrededor de los 12 años. Es raro que estos episodios ocurran por primera vez en la edad adulta, en cuyo caso debe sospecharse que el individuo esté consumiendo alguna sustancia o que haya una enfermedad neurológica subyacente.
El sonambulismo tiene una incidencia familiar. Hasta el 80 % de los individuos sonámbulos presenta antecedentes familiares de sonambulismo o terrores nocturnos, y aproximadamente el 10-20 % de los sonámbulos tiene algún pariente de primer grado con sonambulismo. El riesgo de sufrir este trastorno aumenta todavía más, llega a afectar al 60 % de la descendencia cuando ambos padres tienen antecedentes de haberlo padecido. Se ha sugerido una transmisión de tipo genético, aunque todavía no se conoce el mecanismo exacto de esta transmisión.
La categoría parasomnia no especificada se reserva para las alteraciones caracterizadas por comportamientos o reacciones fisiológicas de carácter anormal que aparecen durante el sueño o en las transiciones sueño-vigilia y que no reúnen los criterios diagnósticos para una parasomnia más específica. Los ejemplos incluyen:
Actividad motora, a menudo de carácter violento, que aparece durante el sueño REM. A diferencia del sonambulismo, estos episodios tienden a hacer acto de presencia en la segunda mitad de la noche y se asocian a recuerdos vívidos del sueño.
Incapacidad para realizar movimientos voluntarios durante la transición entre el sueño y la vigilia. Estos episodios pueden aparecer al acostarse (hipnagógicos) o al despertar (hipnopómpicos) y suelen asociarse a una ansiedad extrema y, en algunos casos, a sensación de muerte inminente. La parálisis del sueño es un síntoma que acompaña con frecuencia a la narcolepsia y, en estos casos codificandose juntos.
En concreto, estos trastornos conllevan la activación del sistema nervioso vegetativo, del sistema motor o de los procesos cognoscitivos durante el sueño o las transiciones sueño-vigilia. Cada parasomnia afecta una fase característica del sueño, de forma que a menudo cada tipo específico de parasomnia incide en una fase de sueño concreta. Las personas con parasomnias suelen acudir a la consulta debido a comportamientos extraños durante el sueño más que por quejas de insomnio o somnolencia diurna excesiva. Comprenden a estas Parasomnias: las pesadillas, los terrores nocturnos, el sonambulismo y la parasomnia no especificada.
Pesadillas
La característica esencial de este trastorno es la aparición repetida de sueños terroríficos que despiertan al individuo, pasando éste a un estado totalmente vigil. Los sueños terroríficos o la interrupción sistemática del descanso nocturno provocan un malestar clínicamente significativo o un deterioro social o laboral. Este diagnóstico no debe efectuarse si las pesadillas aparecen exclusivamente en el transcurso de otro trastorno mental o se deben a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
Las pesadillas toman la forma típica de un sueño largo y elaborado que provoca una intensa ansiedad o terror. El contenido de estos sueños suele centrarse en peligros físicos inminentes para el individuo. Las pesadillas que aparecen después de experiencias traumáticas pueden recrear esta situación original, si bien la mayoría de ellas no hacen referencia a acontecimientos reales. Al despertar, los individuos con este trastorno son capaces de describir la secuencia del sueño con detalle; a veces relatan haber tenido múltiples pesadillas en una misma noche, a menudo centradas en un tema recurrente.
Las pesadillas aparecen casi exclusivamente en el sueño REM, y, como estos episodios REM ocurren de forma periódica a lo largo del sueño nocturno, aproximadamente cada 90-110 min., las pesadillas pueden estar en cualquier momento de la noche. No obstante, como los períodos de sueño REM se hacen típicamente prolongados y el componente onírico adquiere más intensidad en la segunda mitad de la noche, las pesadillas también tienen más probabilidades de aparecer en esta segunda mitad.
Las pesadillas suelen terminar con el despertar del individuo, que se asocia a un rápido retorno al estado de plena alerta y a una sensación prolongada de miedo o ansiedad. Sin embargo, si los despertares nocturnos son frecuentes o el individuo evita dormir por miedo a las pesadillas, puede aparecer somnolencia excesiva, dificultades para la concentración, depresión, ansiedad o irritabilidad.
En estos individuos son frecuentes los síntomas de depresión o ansiedad que no reúnen los criterios diagnósticos de un trastorno específico. Debido a la pérdida de tono muscular característica del sueño REM, es raro que aparezcan movimientos corporales o vocalizaciones.
Las palabras, gritos o sacudidas suelen ser un fenómeno de breve duración que anuncia el final de la pesadilla y son más característicos de las pesadillas que acompañan al trastorno por estrés postraumático, ya que éstas tienen lugar en el sueño NREM.
Terrores nocturnos
La característica esencial de este trastorno es la aparición repetida de terrores nocturnos, es decir, despertares bruscos que suelen estar precedidos por gritos o lloros de angustia.
Los terrores nocturnos suelen hacer acto de presencia durante el primer tercio del sueño y prolongarse por espacio de 1-10 min. Estos episodios se acompañan de activación vegetativa y manifestaciones comportamentales de miedo intenso. Durante el episodio, es difícil despertar o calmar al individuo. De todas formas, si éste consigue despertarse, no recuerda nada del contenido del terror o bien sólo imágenes fragmentadas y aisladas. Al levantarse por la mañana, es típica la amnesia sobre lo acontecido durante la noche. Los episodios de terror nocturno provocan un malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo.
Es típico que durante uno de estos episodios el individuo se siente bruscamente en la cama y empiece a gritar o a llorar, mostrando una expresión facial de terror y signos vegetativos de intensa ansiedad como taquicardia, taquipnea, enrojecimiento, sudoración, dilatación pupilar, aumento del tono muscular. El individuo no suele responder a los esfuerzos de los demás por despertarlo o calmarlo. Si por fin logra despertarse, se muestra confuso y desorientado durante unos minutos y describe una vaga sensación de terror, a menudo sin componente onírico asociado.
Los individuos con trastorno por estrés postraumático y el trastorno de ansiedad generalizada, tienen asimismo un riesgo mayor de padecer terrores nocturnos. Los individuos con terrores nocturnos, por su parte, pueden presentar trastornos de la personalidad, en especial trastornos dependiente y límite de la personalidad. Los tests e inventarios de personalidad practicados en estos individuos arrojan altas puntuaciones para la depresión y la ansiedad.
Sonambulismo
La característica esencial del sonambulismo es la existencia de episodios repetidos de comportamientos motores complejos que se inician durante el sueño y que implican que el individuo se levante de la cama y empiece a andar. Los episodios de sonambulismo suceden durante las fases de sueño con actividad EEG lenta y, por tanto, suelen aparecer en el primer tercio de la noche. Durante estos episodios, el individuo presenta una disminución del estado vigil y de la reactividad a los estímulos, mirada fija y perdida, y una ausencia relativa de respuesta al diálogo o a los esfuerzos que emprenden los demás para despertarlo. Si logra despertarse durante uno de estos episodios, el individuo no consigue recordarlo con claridad. Después del episodio, puede aparecer un breve período de confusión en un primer momento, que suele seguirse de una recuperación total de las funciones cognoscitivas y del comportamiento normal. El sonambulismo debe provocar malestar clínicamente significativo. No debe establecerse el diagnóstico de sonambulismo si el comportamiento que lleva a cabo el individuo por la noche se debe a los efectos fisiológicos directos de una sustancia o de una enfermedad médica.
Los episodios de sonambulismo pueden terminar en forma de despertar espontáneo que se sigue de breves períodos de confusión; en otras ocasiones el individuo vuelve a acostarse y sigue durmiendo como si nada hubiera pasado. No es raro que a la mañana siguiente el individuo se despierte en otros lugares o encuentre pruebas de haber llevado a cabo algunas actividades durante la noche, aunque de todas formas la amnesia preside el recuerdo de estos acontecimientos. La articulación de la palabra es pobre, y es raro que se establezcan diálogos, pueden obedecer los requerimientos de otras personas para que cesen en su actividad y retornen a la cama. De todas formas, todos estos comportamientos están presididos por un bajo nivel de vigilancia, de modo que despertar al sujeto en pleno episodio resulta característicamente muy difícil. Si logra despertarse, permanece confuso durante unos minutos y posteriormente recupera el estado de vigilia normal.
Los individuos con sonambulismo pueden presentar asimismo otras parasomnias asociadas al sueño NREM como son los terrores nocturnos. En los niños el sonambulismo no suele coexistir con otros trastornos mentales, pero en los adultos esto sí puede suceder, sobre todo con trastornos de la personalidad, trastornos del estado de ánimo o trastornos de ansiedad.
El sonambulismo incide por igual en varones y mujeres. La máxima prevalencia se sitúa alrededor de los 12 años. Es raro que estos episodios ocurran por primera vez en la edad adulta, en cuyo caso debe sospecharse que el individuo esté consumiendo alguna sustancia o que haya una enfermedad neurológica subyacente.
El sonambulismo tiene una incidencia familiar. Hasta el 80 % de los individuos sonámbulos presenta antecedentes familiares de sonambulismo o terrores nocturnos, y aproximadamente el 10-20 % de los sonámbulos tiene algún pariente de primer grado con sonambulismo. El riesgo de sufrir este trastorno aumenta todavía más, llega a afectar al 60 % de la descendencia cuando ambos padres tienen antecedentes de haberlo padecido. Se ha sugerido una transmisión de tipo genético, aunque todavía no se conoce el mecanismo exacto de esta transmisión.
Parasomnia no especificada
La categoría parasomnia no especificada se reserva para las alteraciones caracterizadas por comportamientos o reacciones fisiológicas de carácter anormal que aparecen durante el sueño o en las transiciones sueño-vigilia y que no reúnen los criterios diagnósticos para una parasomnia más específica. Los ejemplos incluyen:
Trastorno comportamental del sueño REM
Actividad motora, a menudo de carácter violento, que aparece durante el sueño REM. A diferencia del sonambulismo, estos episodios tienden a hacer acto de presencia en la segunda mitad de la noche y se asocian a recuerdos vívidos del sueño.
Parálisis del sueño
Incapacidad para realizar movimientos voluntarios durante la transición entre el sueño y la vigilia. Estos episodios pueden aparecer al acostarse (hipnagógicos) o al despertar (hipnopómpicos) y suelen asociarse a una ansiedad extrema y, en algunos casos, a sensación de muerte inminente. La parálisis del sueño es un síntoma que acompaña con frecuencia a la narcolepsia y, en estos casos codificandose juntos.
Consiste en alteraciones del sueño debidas a un trastorno mental diagnosticable (a menudo trastornos del estado de ánimo o trastornos de ansiedad), que es de suficiente gravedad como para merecer atención clínica independiente. La característica esencial de estos trastornos es la presencia de insomnio o hipersomnia que se considera temporal y etiológicamente relacionada con otro trastorno mental. El insomnio o la hipersomnia que se deben a los efectos fisiológicos directos de una sustancia no se incluyen aquí y deben ser diagnosticados como trastorno del sueño inducido por sustancias.
El insomnio relacionado con otro trastorno se caracteriza por dificultades para conciliar el sueño, despertares frecuentes o sensación acusada de sueño no reparador durante por lo menos 1 mes y se asocia a fatiga diurna o afectación de la actividad diaria del individuo. La hipersomnia relacionada con otro trastorno mental se caracteriza por sueño nocturno prolongado o episodios repetidos de sueño diurno durante al menos 1 mes. En ambos trastornos estas alteraciones provocan malestar clínicamente significativo o deterioro social, laboral o de otras áreas importantes de la actividad del individuo. El insomnio o la hipersomnia no se explican mejor por la presencia de otro trastorno mental ni por sueño insuficiente. Estas alteraciones del sueño no se deben a los efectos fisiológicos directos de una sustancia.
Las alteraciones del sueño son características frecuentes de otros trastornos mentales. Sólo debe efectuarse el diagnóstico de insomnio o hipersomnia relacionados con otro trastorno mental cuando estas alteraciones del sueño sean uno de los principales motivos de consulta y revistan la suficiente gravedad como para merecer una atención clínica independiente. Los individuos con alguno de estos trastornos suelen dar la máxima importancia a sus alteraciones del sueño, y ello puede enmascarar los síntomas característicos del trastorno mental subyacente; a veces sólo un interrogatorio detallado lo pondrá de relieve.
Muchos trastornos mentales pueden producir insomnio o hipersomnia, convirtiéndose éstos en motivos principales de consulta. En el trastorno depresivo mayor los individuos suelen aquejar dificultad para conciliar o mantener el sueño, o despertar precoz sin poder volver a dormirse. La hipersomnia relacionada con trastornos del estado de ánimo se asocia a menudo a trastorno bipolar del estado de ánimo, con episodio más reciente depresivo, o a un episodio depresivo mayor con síntomas atípicos. En el trastorno de ansiedad generalizada los individuos suelen manifestar dificultades para conciliar el sueño y despertarse a medianoche con ideas recurrentes de ansiedad hasta presentar crisis de angustia nocturnas que pueden desembocar en insomnio.


